按要求填空:
(1)0.2molO3和0.3molO2的质量 (选填“相等”、“不相等”或“无法判断”),分子数之比为 ,所含原子数之比为 ,在相同条件下的体积之比为 。
(2)73g HCl气体中含有 个分子,标准状况下占有的体积为 L。
(3)相同物质的量浓度的KCl、CuCl2、AlCl3溶液,分别与AgNO3溶液反应,当生成的AgCl沉淀的质量之比为3︰2︰1时,三种溶液的体积比为 。
(4)标准状况下V L氯化氢气体溶解在1L水中,所得溶液的密度为ρg/mL,溶液中溶质的质量分数为ω,物质的量浓度为c mol/L,则ω= (任写一种表达式)。
摩尔盐是硫酸盐中带有结晶水的一种复盐,是一种重要化工原料,其组成可通过下列实验测定:定性检验:①配制莫尔盐的溶液,取它的水溶液,加入KSCN不显红色,再滴入几滴新制氯水溶液显红色;另取莫尔盐溶液,逐滴加入NaOH溶液,发现反应生成白色沉淀A,很快沉淀颜色发生改变,继续滴加NaOH溶液,又发现沉淀逐渐增多,继续滴加至过量后沉淀又部分溶解,最终生成沉淀B。
定量测定:②称取1.8520 g样品,准确配成100 mL溶液A;
③量取25.00 mL溶液A,加入盐酸酸化的BaCl2溶液至沉淀完全,过滤、洗涤,干燥至恒重,得到白色固体0.4660 g;
④再量取25.00 mL溶液A,滴加适量稀硫酸,用0.0100 mol·L-1KMnO4溶液滴定至终点,生成Mn2+,消耗KMnO4溶液10.00 mL。
请回答一下问题:
(1)写出①中物质的化学式A ,B ;
(2)已知室温下BaSO4的Ksp=1.1×10-10,欲使溶液中c(SO42-)≤1. 0×10-5mol·L-1,则应保持溶液中c(Ba2+)≥ mol·L-1;
(3)③中发生反应的离子方程式为 ,滴定终点的现象是 ;
(4)通过计算确定样品的组成(必须写出计算过程)。
四氧化三铁是一种常用的磁性材料,纯净的四氧化三铁用来作录音磁带和电讯器材的原材料。下图是氧化沉淀法生产Fe3O4工艺流程示意图: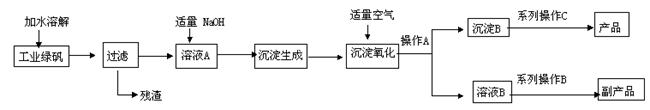
已知:①工业绿矾中的杂质不溶于水,不参与反应;②Fe(OH)2 +2Fe(OH)3 =Fe3O4 +4H2O 。
请回答下列问题:
(1)铁的常见氧化物中可用作颜料的化学式是 。
(2)加水溶解过程中,实验室通常使用的玻璃仪器有 ,操作A的名称是 ,与加水溶解的过程中用到不同的玻璃仪器是 。
(3)在工艺流程中,通入适量空气氧化时的化学方程式为 。
(4)由溶液B获得该副产品要经历以下步骤,请排出正确的操作顺序是 (填字母编号),得到副产品的化学式为 。
a.过滤 b.加热浓缩 c.结晶 d.冷却 e.洗涤
(5)Fe3O4与稀硝酸恰好完全反应时,氧化剂与还原剂的物质的量之比为 。
有A、B、C、D、E五种元素,它们的原子序数均不大于20,且原子序数依次递增。A是元素周期表所有元素原子半径最小的;B只有两个电子层,B中两层电子数之和是两层电子数之差的三倍;C和D分别位于同主族,且D中最外两电子层电子数之差等于最内层电子数;E核外最外层电子数与最内层电子数相等。
请按要求回答下列问题:
(1)A2C和A2D的沸点较高者为 (填化学式),写出由A和C组成的含有非极性健的化合物的电子式 ;
(2)由上述元素组成的化合物中属于极性健构成的非极性分子是(只要求写出两种,用化学式表示) ;
(3)由C与E形成的化合物高温时与B形成的物质反应生成两种化合物,请写出该反应的化学方程式: ;
(4)写出上述元素形成的化合物中一种可溶性的正盐与另一种强酸反应的离子方程式:
;
(5)上述元素形成的化合物中通常能污染空气(至少写出2种) 。
【化学—选修5 有机化学基础】
绿原酸(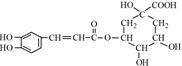 )是一种抗氧化药物,存在下图转化关系。
)是一种抗氧化药物,存在下图转化关系。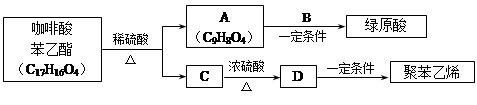
(1)绿原酸中的含氧官能团有: 。
(2)B的分子式是 。
(3)C的氧化产物能发生银镜反应,则C→D的化学方程式是 。
(4)咖啡酸苯乙酯的结构简式是 。
(5)F是A的同分异构体。F分别与碳酸氢钠溶液或新制Cu(OH)2反应产生气体或红色沉淀;苯环上只有两个取代基,且核磁共振氢谱表明该有机物中有8种不同化学环境的氢。
①符合上述条件的F有 种可能的结构。
②若F还能与NaOH在常温下以物质的量之比1∶2完全反应,其化学方程式是
(任写1个)。
【化学—选修3物质结构与性质】
(1)写出Fe2+离子基态的电子排布式:__________________________________。
(2)PO43‾的空间构型是:___________________________________________。
(3)CN-与N2是等电子体,则CN-中C原子的杂化方式是:_______________。
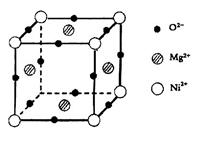
(4)六方氮化硼(BN)晶体具有很高的熔点,B原子和N原子均为sp2杂化。该 晶体中存在的作用力有:__________________。
(5)元素O、Mg、Ni可形成一种晶体,其晶胞如图所示。在晶体中,每个Ni2+离子与_____________个Mg2+离子配位。该晶体的化学式是____________。