若NA表示阿伏加德罗常数的值,下列叙述正确的是
①标准状况下,2.24 L四氯化碳含碳原子数为0.1NA
②标准状况下,a L的氧气和氮气的混合物含有的原子数为2 a NA /22.4
③电解精炼铜时,若阴极得到电子数为2NA个,则阳极质量减少64 g
④7 g CnH2n中含有的氢原子数为2NA
⑤常温常压下,7.1g氯气与足量的氢氧化钠溶液反应转移的电子数为0.1NA
⑥1 L 2 mol·L-1 FeCl3溶液中含Fe3+数为2NA
⑦2 L1 mol·L-1的盐酸中所含氯化氢分子数为2NA
| A.①④⑦ | B.②⑥ | C.③④⑤ | D.②⑤ |
A、B、C、D、E是核电荷数依次增大的五种短周期元素,原子半径按D、E、B、C、A的顺序依次减小,B和E同主族,则下列推断中不正确的是( )
A.A、B、E一定各在不同周期
B.A、D可能在同一主族
C.C的最高正价氧化物对应的水化物可能显碱性
D.C和D的单质可能化合形成离子化合物
下列外围电子排布式(或外围轨道表示式)的原子中,第一电离能最小的是( )
A.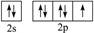 |
B.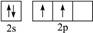 |
| C.3d64s2 | D.6s1 |
X与Y两元素的阳离子具有相同的电子层结构,X元素的阳离子半径大于Y元素的阳离子半径,Y与Z两元素的核外电子层数相同,Z元素的第一电离能大于Y元素的第一电离能,则X、Y、Z的原子序数( )
| A.X>Y>Z |
| B.Y>X>Z |
| C.Z>X>Y |
| D.Z>Y>X |
下列说法中错误的是( )
| A.所有的非金属元素都分布在p区 |
| B.元素周期表中ⅢB族到ⅡB族10个纵行的元素都是金属元素 |
| C.除氦以外的稀有气体原子的最外层电子数都是8 |
| D.同一元素的各种同位素的化学性质一定相同 |
将等体积的硫化钠溶液与亚硫酸钠溶液混合,并加入适量硫酸,有黄色沉淀产生,微热,无酸性气体产生,则原混合液中Na2S与Na2SO3的物质的量之比是( )
| A.3∶2 | B.1∶2 |
| C.2∶1 | D.1∶1 |