已知氧化还原反应发生的条件是:氧化性:氧化剂>氧化产物,还原性:还原剂>还原产物。又已知还原性强弱顺序是I->Br—>Fe2+>Cl-(氧化性Cl2>Fe3+>Br2>I2),下列反应的化学方程式或叙述不成立的是( )
| A.Br2+2HI = I2+2HBr |
| B.2FeCl2+Cl2=2FeCl3 |
| C.2FeCl2+2HCl+I2=2FeCl3+2HI |
| D.Cl2通入到NaBr和NaI的混合溶液中:Cl2优先氧化I- |
通过控制或改变反应条件可以加快、减缓甚至阻止反应的进行,使化学反应有利于人类的生存和提高生活质量。下列图示的措施中,是为了加快化学反应速率的是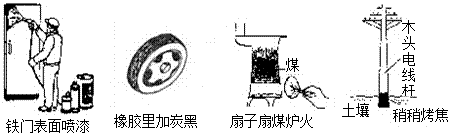
A B C D
2005年4月22日是第36个“世界地球日”,我国国土资源部确定的主题为“善待地球科学发展,构建和谐”。下列行为不符合活动主题的是
| A.更新采煤、采油技术,提高产量以满足工业生产快速发展的需要 |
| B.控制含磷洗涤剂的使用,防止水体富营养化,保护水资源 |
| C.开发太阳能、水能、风能、可燃冰等新能源,减少使用煤、石油等化石燃料 |
| D.落实资源的“3R”发展观,即减少资源消耗(Reduce)、增加资源的重复使用(Reuse)、资源的循环再生(Recycle) |
在一定温度下,反应A2(g)+B2(g) 2AB(g)达到反应限度的标志是
2AB(g)达到反应限度的标志是
A、容器内气体的总压强不随时间变化而变化
B、A2、B2和AB的物质的量不再改变
C、c(A2):c(B2):c(AB)===1:1:2
D、A2和B2的物质的量之和与AB的物质的量相等
aXn-和bYm+为两主族元素的离子, 它们的电子层结构相同, 下列判断错误的是
| A.原子半径X<Y | B.a+n="b-m" |
| C.Y最高价氧化物的化学式为YOm | D.X的氢化物的化学式为HnX |
下列分子中,所有原子都满足最外层为8电子结构的是
| A.CO2 | B.SiH4 | C.SF6 | D.PCl5 |