某温度下,在2 L容器中3种物质间进行反应, X、Y、Z的物质的量随时间的变化曲线如图。反应在t1 min时到达平衡,依图所示:
⑴①该反应的化学方程式是_____________________。
②在t1 min时,该反应达到了__________状态,下列可作为判断反应已达到该状态的是__________
| A.X、Y、Z的反应速率相等 |
| B.X、Y的反应速率比为2︰3 |
| C.生成3 mol Y的同时生成1 mol Z |
| D.生成1 mol Z的同时生成2 mol X |

 ⑵①若上述反应中X、Y、Z分别为NH3、H2、N2,且已知1 mol氨气分解成氮气和氢气要吸收46 kJ的热量,则至t1 min时,该反应吸收的热量为:__________;在此t1 min时间内,用H2表示反应的平均速率v(H2)= __________。
⑵①若上述反应中X、Y、Z分别为NH3、H2、N2,且已知1 mol氨气分解成氮气和氢气要吸收46 kJ的热量,则至t1 min时,该反应吸收的热量为:__________;在此t1 min时间内,用H2表示反应的平均速率v(H2)= __________。 ②两位同学讨论放热反应和吸热反应。甲说加热后才能发生的化学反应是吸热反应,
②两位同学讨论放热反应和吸热反应。甲说加热后才能发生的化学反应是吸热反应, 乙说反应中要持续加热才能进行的反应是吸热反应。你认为他们说法正确的是______同学。
乙说反应中要持续加热才能进行的反应是吸热反应。你认为他们说法正确的是______同学。
(1)一定温度下,在恒容密闭容器中N2O5可发生下 列反应:2N2O5(g)
列反应:2N2O5(g)  4NO2(g)+O2(g) ;⊿H>0
4NO2(g)+O2(g) ;⊿H>0
①反应达到平衡后,若再通入一定量氮气,则N2O5的转化率将(填“增大”、
“减小”或“不变”)。
②下表为反应在T1温度下的部分实验数据:
| t/s |
0 |
500 |
10 00 00 |
| c(N2O5)/mol·L—1 |
5.00 |
3.52 |
2.48 |
则500s内N2O5的分解速率为。
③在T2温度下,反应1000s时测得NO2的浓度为4.98mol/L,则T2T1。(填“>”、“<” 或 “ =”)
(2)如图所示装置可用于制备N2O5,则N2O5在电解池的区 (填“阳极”或“阴极”)生成,其电极反应式为。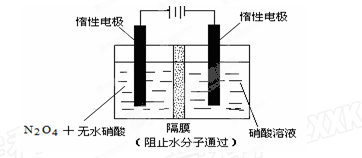
铅蓄电池是典型 的可充型电池,它的正负极格板是惰性材料,电池总反应式为:
的可充型电池,它的正负极格板是惰性材料,电池总反应式为:
Pb+PbO2+4H++2SO2-4 2PbSO4+2H2O
2PbSO4+2H2O
请回答下列问题(不考虑氢、氧的氧化还原)
①放电时:正极的电极反应式是______________;电解液中H2SO4的浓度将变________;当外电路通过1 mol电子时,理论上负极板的质量增加________g。
②在完全放电耗尽PbO2和Pb时,若按题图连接,电解一段时间后,则在A电极上生成__________、B电极上生成________,此时铅蓄电池的正负极的极性将___。(填“不变”或“对换”)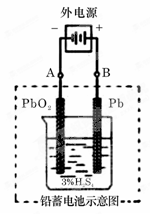
某地区用含较多Ca2+,Mg2+的天然水按照下列步骤制取蒸馏水。请回答下列问题。步骤:天然水→①沉降→②过滤→③曝气→④离子交换→⑤消毒→纯净水
(1)该地区的天然水属于(“硬水”或“软水”)。
(2)在第①步中需要加入凝聚剂,常用的凝聚剂可以是。
(3)经过第④步离子交换后要经过杀菌消毒才能直接饮用。常用的消毒方式有。
(4)若采用药剂法软化天然水,可以向其中加入碳酸钠,发生反应的离子反应方程式是
,如果是暂时硬度,可用加热的方法除去,请写出发生的化学反应方程式 (写出一个即可)。
(写出一个即可)。
将锌片和铜片用导线相连后一同插入稀硫酸中,导线上便有电流通过。
(1)锌片为______(填“正极”或“负极”),电极反应是。
(2)铜片为__________(填“正极”或“负极”),发生反应(填“ 氧化”或“还原”)。
氧化”或“还原”)。
(3)该原电池工作时,溶液中的SO42-向极移动,铜极上的现象是。
 下边是日照2
下边是日照2 010年9月11日的空气质量日报
010年9月11日的空气质量日报
| 污染指数 |
首要污染物 |
空气质量级别 |
空气质量状况 |
||
| 二氧化硫 |
二氧化氮 |
可吸入颗粒物 |
|||
| 12 |
33 |
66 |
2 |
良 |
(1)首要污染物是
(2)污染指数是
(3)能引起光化学烟雾的是(从表中选)
(4)能引起酸雨的是(从表中选)