下列离子方程式书写正确的是 
A.金属钠投入水中: Na + H2O Na+ + OH-+ H2↑
Na+ + OH-+ H2↑
B.铜加入稀硝酸中: 3Cu + 8H+ + 2NO3- 3Cu2+ + 2NO↑+ 4H2O
3Cu2+ + 2NO↑+ 4H2O
C.向AlCl3溶液中加入过量氨水: Al3+ + 4NH3• H2O  AlO2-+ 4NH4+ + 2H2O
AlO2-+ 4NH4+ + 2H2O
D NH4HCO3溶液与过量KOH浓溶液共热:NH4++ OH-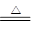 NH3↑+ H2O
NH3↑+ H2O
下列有关周期表的叙述中正确的是
| A.碱土金属元素是指ⅡA族的所有元素 |
| B.除第一周期外,其他周期均有18种元素 |
| C.过渡元素都是副族元素 |
| D.主族元素的原子,半径越大,越容易得到电子 |
所谓合金,就是不同种金属(也包括一些非金属)在熔化状态下形成的一种熔合
物,根据下列四种金属的熔沸点:
| Na |
Cu |
Al |
Fe |
|
| 熔点 |
97.5.C |
1083℃ |
660℃ |
1535℃ |
| 沸点 |
883℃ |
2595℃ |
2200℃ |
3000℃ |
其中不能形成合金的是
A.Cu和Na B.Fe与Cu C.Cu与Al D.Al与Na
从石器、青铜器到铁器时代,金属的冶炼体现了人类文明的发展水平。如图表示了三种金属被人类开发利用的大致年限。之所以有先后,主要取决于
| A.金属的化合价高低 | B.金属的活动性大小 |
| C.金属的导电性强弱 | D.金属在地壳中的含量多少 |
下列反应中,生成物的总能量大于反应物的总能量的是
| A.氢气在氧气中燃烧 | B.焦炭在高温下与水蒸气反应 |
| C.硫在氧气中燃烧 | D.铁丝在氧气中燃烧 |
在下列所表示的微粒中,得电子能力最强的是