下图是实验室中制备气体或验 证气体性质的装置图
证气体性质的装置图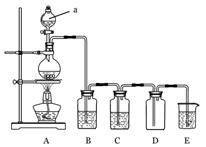
(1)仪器a的名称是_________________。
(2)利用上图装置制备纯净、干燥的氯气。
①圆底烧瓶内发生反应的离子方程式为_______________________________________。
②装置B中的溶液为__________________________;
烧杯中溶液的作用为________________ 。
。
(3)利用上图装置证明SO2具有漂白性、还原性及生成气体中含有CO2。
圆底烧瓶内加入碳,a中加入浓硫酸,B、D中匀为少量品红溶液,C中为足量酸性高锰酸钾溶液,E中为澄清石灰水。
①证明SO2具有漂白性的装置是 ,现象是
②证明SO2具有还原性的现象是
③证明生成气体中含有CO2的现象是
④D装置的作用是 。
分某链烃A的分子式为C6H12,已知其分子中所有的碳原子共平面,且该分子的一氯取代物只有一种,回答下列问题:
(1)A的结构简式为;下列物质与A以任意比例混合,若总物质的量一定,充分燃烧消耗氧气的量相同的是。(填序号)。
A、C7H12O2 b、C6H14 C、C6H14O D、C7H14O3
(2)A与Br2的CCl4溶液反应生成B,B与NaOH的醇溶液共热可得到D,D分子中无溴原子。请写出由B制备D的化学反应方程式:。
(3)B与足量NaOH水溶液完全反应,生成有机物E。
①E可能发生的反应类型有。(填序号)
A、取代反应 B、消去反应 C、加聚反应 D、还原反应
②E与乙二醇的关系是。(填序号)
A、同分异构体 B、同系物 C、同一物质 D、同素异形体
(4)E与乙二酸在一定条件下生成分子式为C8H12O4的有机物,请写出该反应的化学方程式
。
分有A、B两种烃,其相关信息如下:
| A |
①完全燃烧的产物中n(CO2):n(H2O)=2:1 ②28<M(A)<60 ③不能使溴的四氧化碳溶液褪色 ④一氯代物只有一种结构 |
| B |
①饱和链烃,通常情况下呈气态 ②有同分异构体 ③二溴代物有三种 |
回答下列问题:
(1)烃A的实验式是。
(2)烃A的化学式是。
(3)烃B的二溴代物的结构简式为(写一种)。
(4)每断开A中的1mol C—C键,并加成1 mol H2,吸收热量 a kJ,则1 mol A转化为B,需吸收的热量为kJ。
分已知有机物甲、乙、丙有如下信息:
| 甲 |
乙 |
丙 |
|
| 所含元素 |
C、H |
C、H、F |
C、H、F |
| 所含电子数 |
26 |
||
| 结构特点 |
饱和有机物 |
据此推断:
(1)甲的分子式为,若甲分子中有2个氢原子被F原子取代,所得的有机产物可能有种。
(2)乙是性能优良的环保产物,可代替某些破坏臭氧层的氟利昂产品用作制冷剂。其分子中C、H、F的原子个数之比为1:2:2,则乙的结构式为。下列关于乙的叙述正确的是。
A.其分子构型为正四面体形 B.它能使溴水褪色
C.1 mol 乙最多能与1 mol F2发生取代反应 D.它没有同分异构体
(3)将甲、乙按物质的量之比1:1混合,所得混合物的平均摩尔质量等于丙的摩尔质量,且丙分子不存在同分异构体,则丙的分子式为。
将等物质的量的A、B混合于2 L的密闭容器中,发生如下反应: 3A(g)+B(g) xC(g)+2D(g),经5 min后,测得D的浓度为0.5 mol/L,c (A)∶c(B)=3∶5,C的平均反应速率为0.1 mol/(L·min)。求:
xC(g)+2D(g),经5 min后,测得D的浓度为0.5 mol/L,c (A)∶c(B)=3∶5,C的平均反应速率为0.1 mol/(L·min)。求:
(1)此时A的浓度c(A)=________mol/L,反应开始前容器中的A、B的物质的量:n(A)= n(B)=________mol;
(2)B的平均反应速率v(B)=________mol/(L·min);
(3)x的值为________。
下表是元素周期表的一部分, 针对表中的①~⑨种元素,填写下列空白:
| 主族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0族 |
| 2 |
① |
② |
③ |
|||||
| 3 |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
|||
| 4 |
⑨ |
(1)在这些元素中,化学性质最不活泼的是:_____________ (填具体元素符号,下同)。
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是_______,碱性最强的化合物的电子式是:_____________。
(3)最高价氧化物是两性氧化物的元素是_____________;写出它的氧化物与氢氧化钠反应的离子方程式____________________________________________。
(4)用电子式表示元素④与⑥形成的的化合物的形成过程_________________________ ,该化合物属于__________________(填 “共价”或“离子”)化合物。
(5)元素①与⑦形成的的化合物的电子式为______________________,该化合物是由___________ (填“极性”“非极性”)键形成的。