水是生命的源泉,也是不可缺少的资源。
(1)某矿泉水的主要矿物质成分及含量如下表:
| 成分 |
Ca |
K |
Zn |
F |
| 含量(mg/L) |
20 |
3 |
0.06 |
0.02 |
这里Ca、K、 Zn、F是指 (填“单质、元素、分子或原子”)。
(2)水污染日益严重,水资源的保护和合理利用已受到人们的普遍关注。请参与讨论下列有关问题:
(Ⅰ)自来水、蒸馏水、海水中属于纯净物的是 。
(Ⅱ)某学校饮水处可以将自来水净化为饮用水,其中处理步骤如下图所示: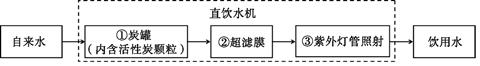
①对应的作用是 (填字母序号,下同),③对应的作用是 。
A.杀菌消毒 B.吸附杂质 C.沉淀过滤 D.蒸馏
(Ⅲ)下列做法会造成水体污染的有 。
A.工业废水直接排放 B.工业废气处理后排放
C.禁止使用含磷洗衣粉 D.大量使用化肥、农药
(Ⅳ)能确认水是由氧元素和氢元素组成的实验是 。
A.氢气在氧气中燃烧生成水 B.水的蒸发
C.水的电解 D.水的净化
已知浓硝酸是一种易挥发的强酸,见光易分解,其分解的反应方程式:
4HNO3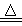 2H2O + 4NO2 ↑ + X ↑
2H2O + 4NO2 ↑ + X ↑
根据上述信息,回答下列问题:
(1)浓硝酸的化学性质有(写出一种即可)
(2)水中氢、氧元素的质量比是(最简整数比)
(3)X的化学式是
(4)二氧化氮分子由氮原子和氧原子构成,其中,氮原子的原子结构示意图为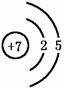
氮原子的最外层电子数为。
根据下列粒子结构示意图,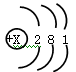
回答问题:
(1)图中X=,该原子的元素符号是。
(2)在元素周期表中。该元素的原子序数为。
(3)在该元素与氯元素组成的化合物中,该元素显(选填“正价”或“负价”)
根据物质的变化和性质回答下列问题。
(1)2014年1月6日,在辽宁省沈阳市皇姑区,一栋房屋因自来水管爆裂形成“冰瀑”景观。这一过程发生的是。(填“物理变化”或“化学变化”)
(2)三聚氰胺在一般情况下较稳定,与盐酸、硫酸、硝酸、乙酸等都能形成三聚氰胺盐。这句话描述的是三聚氰胺的。(填“物理性质”或“化学性质”)
下表是研究性学习小组研究影响过氧化氢(H2O2)分解速率的因素时采集的一组数据:
请你分析回答:用10mL H2O2制取150mL所需的时间(秒)
| 反应条件 \浓度 |
30% H2O2 |
15% H2O2 |
10% H2O2 |
5% H2O2 |
| 无催化剂、不加热 |
几乎不反应 |
几乎不反应 |
几乎不反应 |
几乎不反应 |
| 无催化剂、加热 |
360 |
480 |
540 |
720 |
| MnO2催化剂、加热 |
10 |
25 |
60 |
120 |
该研究小组在设计方案时。考虑了浓度_________、__________等因素对过氧化氢分解速率的影响。
现有以下仪器,请回答下列问题:
(1)仪器⑤的名称是;取用粉末状固体必须用到的仪器是(填序号)。
(2)如果用加热高锰酸钾的方法制取氧气,制气装置(即反应装置)应选仪器(填序号);收集氧气的方法有和 。
(3)如果用过氧化氢溶液分解来制取氧气,制气装置(即反应装置)最好选用仪器(填序号)
(4)比较(2)和(3)两种制取氧气的方法,最好选用方法(3)的原因是。
(5)把上面分解KMnO4制取氧气的仪器装配好后,检验该装置气密性的操作方法为:
。
(6)实验室里用加热高锰酸钾的方法制取氧气,并用排水法收集氧气实验时,待气泡放出时,不宜立即收集,其原因是 ;应待 时,再收集。实验结束时应先把导管 ,后熄灭,原因是 ;集满氧气的集气瓶应放在桌上并盖上玻璃片。
(7)检验O2是否已经集满的方法是。