下列反应的离子反应方程式正确的是:
| A.实验室用氨水、氯化铁溶液制备少量Fe(OH)3:Fe3++ 3OH-==Fe(OH)3↓ |
| B.Ba(OH)2和MgSO4溶液混合:Ba2++ SO42-= BaSO4↓ |
| C.少量二氧化硫气体通入次氯酸钠溶液中:SO2+3ClO-+H2O==SO42-+Cl-+2HClO |
| D.碳酸氢钠溶液与过量澄清石灰水反应 2HCO3-+Ca2++ 2OH- ==CaCO3↓+2H2O +CO32- |
NA为阿伏加德罗常数,下列物质所含分子数最少的是
A.0.8 mol氧气 |
B.标准状况下2.24L氨气 |
| C.3.6g水(水的摩尔质量为18g·mol-1) | D.含NA个氢分子的氢气 |
下列事故或药品的处理正确的是
| A.少量浓硫酸沾在皮肤上,立即用氢氧化钠溶液冲洗 |
| B.眼睛里溅进了少量酸或碱溶液,要立即用大量水冲洗,边洗边眨眼睛 |
| C.不慎洒出的酒精在桌上燃烧起来,应立即用水扑灭 |
| D.将含硫酸的废液倒入水槽,用水冲入下水道 |
危险化学品要在包装标签上印有警示性标志。氢氧化钠应选用的标志是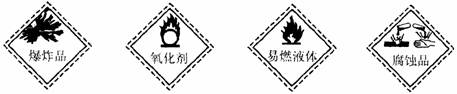
A B C D
国际上曾把原定在2000年全球禁用氟利昂(冰箱制冷剂)的时间提前到1996年,主要是为了保护大气平流层中的一种物质不受破坏,这种物质的同素异形体是
| A.O2 | B.H2 | C.N2 | D.O3 |
用下图装置测定水中氢、氧元素的质量比,其方法是分别测定通氢气前后玻璃管的质量差和U型管的质量差,实验测得m(H)∶m(O)>1∶8。下列对导致这一结果的原因的分析中,一定错误的是
| A.Ⅰ、Ⅱ装置之间缺少干燥装置 | B.Ⅲ装置后缺少干燥装置 |
| C.Ⅱ装置中玻璃管内有水冷凝 | D.CuO没有全部被还原 |