①pH=3的CH3COOH溶液;②pH=3的HCl溶液;③pH=11的氨水;④pH=11的NaOH溶液。相同条件下,有关上述溶液的比较中,错误的是
| A.将②、③溶液混合后,pH=7,消耗溶液的体积:②>③ |
| B.①④等体积混合后,溶液显碱性 |
| C.等体积的①、②、④溶液分别与足量铝粉反应,生成H2的量①最大 |
| D.向溶液中加入100mL水后,溶液的pH:③>④>②>① |
对下列反应改变反应物用量,不能用同一个离子方程式表示的是 ( )[来
①NaHCO3溶液与石灰水反应
②Na2SO3溶液与稀盐酸反应
③Si与烧碱溶液反应
④Fe与稀硝酸反应
| A.①②③ | B.①②④ | C.①③④ | D.②③④ |
下列是某同学对相应反应的离子方程式所作的评价,其中评价合理的是()
| 编号 |
化学反应 |
离子方程式 |
评价 |
| ① |
硫酸溶液中 加入Ba(OH)2溶液 加入Ba(OH)2溶液 |
Ba2++SO=BaSO4↓ |
正确 |
| ② |
氧化铝与NaOH溶液反应 |
2Al3++3O2-+2OH-= 2AlO+H2O |
错误,Al2O3不应写成离子形式 |
| ③ |
铁和稀硝酸反应 |
Fe+2H+===H2↑+Fe2+ |
正确 |
| ④ |
等物质的量的FeBr2和Cl2反应 |
2Fe2++2Br +2Cl2=2Fe3++Br2+4Cl- +2Cl2=2Fe3++Br2+4Cl- |
错误,离子方程式中Fe2+与Br-的物质的量之比与化学式不符 |
| A.只有② | B.①③ | C.②④ | D.①②③④ |
在一瓶无色未知溶液中检验出有Ba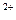 、Ag
、Ag ,同时又测得其酸性很强。某学生还要鉴定此溶液中是否大量存在:①Cu
,同时又测得其酸性很强。某学生还要鉴定此溶液中是否大量存在:①Cu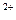 、②Fe
、②Fe 、③ Cl
、③ Cl 、④ NO
、④ NO 、⑤ S
、⑤ S 、⑥ CO
、⑥ CO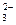 、⑦ NH
、⑦ NH 、⑧ Mg
、⑧ Mg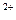 、⑨A1
、⑨A1 、⑩
、⑩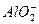 离子。其实,这些离子中有一部分不再鉴定就能加以否定,你认为不必鉴定的离子组是()
离子。其实,这些离子中有一部分不再鉴定就能加以否定,你认为不必鉴定的离子组是()
| A.③⑤⑥⑦⑩ | B.①②⑤⑥⑧⑨ | C.③④⑦⑧⑨ | D.①②③⑤⑥⑩ |
设NA表示阿伏加德罗常数的数值,下列说法正确的是()
| A.2L 1mol·L-1 (NH4)2SO4溶液中含有4NA个铵根离子 |
B.100℃时,1L pH=6的纯水中,含1.0×10-6NA个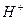 |
| C.电解CuCl2溶液,阴极析出6.4gCu时,转移的电子数为0.1NA |
| D.一定条件下用含1mol FeCl3的溶液制备Fe(OH)3胶体,产生NA个Fe(OH)3胶粒 |
下列物质溶于水时会破坏水的电离平衡,且属于电解质的是()
| A.氯气 | B.二氧化碳 | C.碘化钾 | D.醋酸钠 |