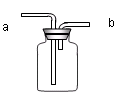
被称为“绿色氧化剂”的过氧化氢(H2O2),俗称双氧水,是一种无色液体,常用作氧化剂、消毒杀菌剂和漂白剂等。在较低温度下和少量催化剂(如MnO2)条件下,它能迅速分解,生成氧气和水。请回答下列问题:
出图1中标号仪器的名称: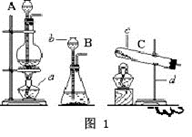
a_________________________
b_________________________
c_________________________
d_________________________
⑵若实验室用过氧化氢代替氯酸钾制取氧气,可采用上面的哪种发生装置?_________(填序号),主要理由是_____________________________。
⑶当过氧化氢接触二氧化锰后,反应便立即开始并不能人为控制其速度。如果稍改变你所选择的装置,便可控制其反应的速度。请从图2的仪器中选择一种仪器更换你选择的装置中的一种仪器,以达到控制反应速度的目的。你选择的仪器是_________________________(填序号,从图2中选择),它更换原装置中的_________________________。(填序号,从图1中选择)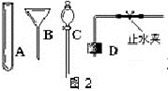
(4)天然气、沼气的主要成分是甲烷(CH4),它是无色无味的气体,密度比空气小,极难溶于水,能燃烧。实验室用无水醋酸钠和碱石灰固体混合物加热制取甲烷气体。若用此法制取甲烷气体,其气体发生装置是_______(从图1 A、B、C中选择),可采用___________法或___________法收集。
下图是A、B、C三种物质的溶解度曲线。
⑴ t2℃时,A、B、C的溶解度从大到小的关系为:;
⑵ t2℃时,把30g A物质与50克水混合,不断搅拌,让A物质充分溶解, 最后所得溶液的质量为;
⑶ t2℃时,A、B、C三者的饱和溶液降温至t1℃后,溶液溶质质量分数保质不变的是;
⑷ 已知A物质中含有少量的B物质,若要提纯A,可采用的方法是。
依据所学化学知识回答:
⑴ 我们常用洗涤剂清洗餐具上的油污,这是因为洗涤剂与油污发生了作用。
⑵ 青少年成长需要充足的钙,这里的“钙”是指钙(填“原子”或“元素”)。
⑶ 不锈钢的主要成分元素为铁、铬(Cr)、镍,铬的表面生成一薄层致密的钝态氧化物保护膜是不锈钢具有耐蚀性的主要原因。请回答下列问题:
① 不锈钢是一种(填“合成材料”或“合金”)。
② 在相同温度下,取大小相同、表面光亮的Cr、Mg、Cu三种金属薄片,分别放入等体积、等溶质的质量分数的足量稀盐酸中,现象如下:
| 金属 |
Cr |
Mg |
Cu |
| 现象 |
放出气泡缓慢 |
放出气泡很快 |
无明显变化 |
则上述三种金属的活动性由强到弱的顺序是。从上述探究实验可知,Cr(填“能”或“不能”)跟CuSO4溶液反应。
维生素C(C6H8O6)主要存在于蔬菜、水果中。近年来科学家发现,维生素C除具有人们所熟知的功效外,还具有防癌作用。但是蔬菜经过高温烹调,Vc将被破坏殆尽,所以一些绿色蔬菜经过油锅快炒即可。
⑴ 以上材料说明维生素C热稳定性(填“好”或“差”);
⑵ 维生素C常被添加入果汁饮料中作为营养增强剂,pH<7时,维C比较稳定,所以在凉拌黄瓜时候可以加入(从“食醋”和“面碱”中选择)作为调料能保持黄瓜营养;
⑶ 维生素C中碳、氧、氢三种元素的质量比是。
从①甲烷②熟石灰③蛋白质④石灰石⑤氢氧化钠⑥盐酸中选择适当物质的序号填空。
⑴ “西气东输”被输送的物质;
⑵ 工业炼铁的原料之一;
⑶ 胃酸的主要成份 ;
⑷ 灼烧会有烧焦羽毛味的物质;
⑸ 易潮解,溶于水时放热的白色固体;
⑹ 常用于改良酸性土壤的物质 。
实验室制取气体所需装置如下图所示,请回答以下问题: 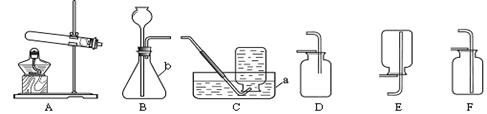
(1)仪器a的名称是____。
(2)用高锰酸钾制取氧气时,所选用的发生装置是_____(填字母序号,下同),用过氧化氢溶液和二氧化锰制取氧气,所选用的发生装置是_____,其化学反应方程式为_____。如果要制得较纯净的氧气应该选择装置_____收集。
(3)实验室选用如下图所示的装置收集二氧化碳,气体应该从端进入,其验满的方法是。