在过去,糖尿病的检测方法是把NaOH溶液和CuSO4溶液加入某病人的尿液中,微热时,如果观察到红色沉淀,说明该尿液中含有
| A.食醋 | B.白酒 | C.食盐 | D.葡萄糖 |
下列说法或表达正确的是
| A.乙醇、糖类和蛋白质都是人体必需的营养物质 |
B.NH4I的电子式: |
| C.石油是混合物,其分馏产品汽油也是混合物 |
| D.陶瓷、水晶、水泥、玻璃都属于硅酸盐 |
高铁酸钾(K2FeO4)是一种兼具净水和消毒功能的可溶性盐,可发生如下反应:
2K2FeO4+16HCl=4KCl+2FeCl3+8H2O+3Q↑,下列说法正确的是
| A.可用湿润的淀粉碘化钾试纸检验产物Q |
| B.K2FeO4在水中的电离方程式为K2FeO4=2K++Fe6++4O2一 |
| C.反应中氧化剂与还原剂的物质的量之比为1:8 |
| D.反应中涉及的6种物质均为电解质 |
下列有关实验的说法正确的是
| A.制氯气时,用饱和碳酸钠溶液和浓硫酸净化气体 |
| B.制少量氧化钠时,将钠置于纯氧中燃烧 |
| C.制二氧化硫时,用浓硫酸干燥气体 |
| D.配制氢氧化钠溶液时,称取一定质量氢氧化钠固体放人容量瓶中并加水至刻度线 |
图像可直观地描述化学反应的进程或结果,下列图像正确的是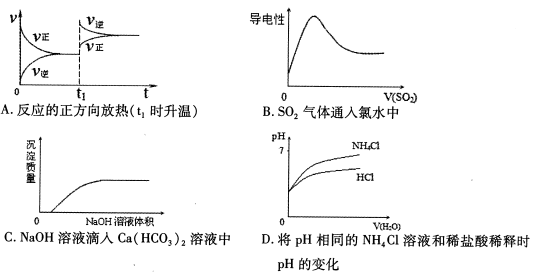
下列物质性质与应用及其对应关系均正确的是
| 选项 |
性质 |
应用 |
| A |
碳酸氢钠可与烧碱反应 |
可用碳酸氢钠作糕点膨松剂 |
| B |
AgCl难溶于稀硝酸 |
可用稀硝酸和AgNO3溶液检测Cl一 |
| C |
浓硫酸具有强氧化性,而稀硫酸的氧化性较弱 |
可用浓硫酸替代稀硫酸与锌反应快速制氢气 |
| D |
碳单质性质稳定 |
可在纯铁中加入少量炭增强抗腐蚀性 |