根据元素周期表和元素周期律分析下面的推断,其中正确的是
| A.锂、钠、钾的原子半径逐渐增大 | B.钠比镁活泼 |
| C.溴单质的氧化性比氯气强 | D.氢氧化钠比氢氧化钾的碱性强 |
化学与科技、生活、环境密切相关,下列说法正确的是①光缆在信息产业中有广泛应用,制造光缆的主要材料是单质硅
②棉、麻、丝、毛及合成纤维完全燃烧都是只生成CO2和H2O
③为防止电池中的重金属污染土壤和水体,应将废电池深埋
④不能将铁制自来水管与铜制水龙头连接
⑤自来水厂在处理水时常加入硫酸铁和氯气,能同时达到消毒杀菌和除去水中悬浮杂质的作用
⑥pH在5.6~7.0之间的降水可通常称为酸雨
⑦汽车尾气中氮氧化物、一氧化碳、碳氢化合物和颗粒物等,严重污染大气
⑧常见的银纪念币制作时一般为铜芯镀银,铜芯应做阳极
| A.①②④⑦⑧ | B.②④⑦⑧ | C.④⑤⑦ | D.②③⑤⑥⑦ |
将1.92gCu和一定量的浓HNO3反应,随着Cu的不断减少,反应生成气体的颜色逐渐变浅,当Cu反应完毕时,共收集到气体1.12L(标准状况),则反应中消耗HNO3的物质的量为
| A.1mol | B.0.05mol | C.1.05mol | D.0.11mol |
标准状况下,将一个充满Cl2的试管倒置于盛有水的水槽中,经过足够长时间的光照后,则试管中主要溶质(设生成物全部留在试管中)的物质的量浓度为
A. mol/L mol/L |
B.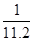 mol/L mol/L |
C.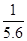 mol/L mol/L |
D.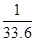 mol/L mol/L |
如图所示,试管中盛装的是红棕色气体(可能是混合物),当倒扣在盛有水的水槽中时,试管内水面上升,但不能充满试管,当向试管内鼓入氧气后,可以观察到试管中水柱继续上升,经过多次重复后,试管内完全被水充满。原来试管中盛装的不可能是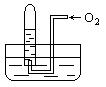
| A.N2与NO2的混和气体 | B.O2与NO2的混和气体 |
| C.NO与NO2的混和气体 | D.NO2气体 |
右图装置中,干燥烧瓶中盛有某种气体a,烧杯和滴管内盛有某种溶液b。挤压滴管的胶头,下列与实验事实不相符的是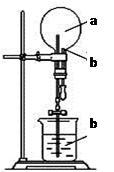
| 气体a |
溶液b |
实验现象 |
|
| A |
SO2 |
NaOH溶液 |
无色喷泉 |
| B |
NH3 |
H2O含紫色石蕊 |
蓝色喷泉 |
| C |
HCl |
H2O含紫色石蕊 |
红色喷泉 |
| D |
C12 |
饱和食盐水 |
无色喷泉 |