氮是地球上含量丰富的元素,氮及其化合物的研究在生产、生活中有着重要意义。
(1)下图是1 mol NO2和1 mol CO反应生成CO2和NO过程中能量变化示意图,写出NO2和CO反应的热化学方程式 。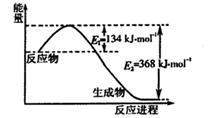
(2)已知:
N2(g)+O2(g)="2" NO(g) △H="+180" kJ·mol-1
2NO(g)+2 CO(g)=N2(g)+2 CO2(g )△H="-746" kJ·mol-1
)△H="-746" kJ·mol-1
则反应CO(g)+1/2O2(g)=CO2(g)的△H= kJ·mol-1
(3)在一固定容积为2L的密闭容器内加人0.2 mol的N2和0.6 mol的H2,在一定条件下发生如下反应。N2(g)+3H2(g) 2NH3(g)△H<0,若第5分钟时达到平衡,此时测得NH3的物质的量为0.2mol,则前5分钟的平均反应速率v(N2)为 ,平衡时H2的转化率为 ,该反应的平衡常数K= 。
2NH3(g)△H<0,若第5分钟时达到平衡,此时测得NH3的物质的量为0.2mol,则前5分钟的平均反应速率v(N2)为 ,平衡时H2的转化率为 ,该反应的平衡常数K= 。
(4)在固定体积的密闭容器中,1.0×103kPa时,反应N2(g)+3H2(g) 2NH3(g) △H<0的平衡常数K与温度T的关系如下表:
2NH3(g) △H<0的平衡常数K与温度T的关系如下表:
| T/K |
298 |
398 |
498 |
| 平衡常数K |
51 |
K1 |
K2 |
则 K1 K2(填写“>”、“=”或“<”)
K1 K2(填写“>”、“=”或“<”)
(5)在体积一定的密闭容器中能说明合成氨反应一定达到平衡状态的是
(填字母)
a. 容器内N2、H2、NH3的浓度之比为1:3:2 b. NH3的浓度保持不变
c. 容器内压强保持不变 d.. 混合气体的密度保持不变
A、B、C、D四种芳香族化合物都是某些植物挥发油中的主要成分,有的是药物,有的是香料。它们的结构简式如下所示:
请回答下列问题:
(1)写出B中官能团的名称;1mol B能与含______molBr2的溴水反应。
(2)既能使FeCl3溶液显紫色又能和NaHCO3反应放出气体的有(用A.B.C.D填空)。
(3)按下图C经一步反应可生成E,E是B的同分异构体,则反应①属于反应(填反应类型名称),写出反应②的化学方程式_______________________________________。
(4)同时符合下列两项要求的D的同分异构体有4种
①化合物是1,2——二取代苯;
②苯环上的两个取代基分别为羟基和含有-COO-结构的基团其中两种(G和H)结构简式如下图所示,请补充另外两种。 、 _____________________,
、 _____________________,
(5)写出H与足量NaOH溶液共热反应的化学方程式
________________________________.
(1)某种混合物中可能含有甲酸、乙酸、甲醇及甲酸乙酯这些物质中的一种或几种。在检验时有以下现象:
(Ⅰ)有银镜反应;
(Ⅱ)加入新制 悬浊液,无变澄清的现象;
悬浊液,无变澄清的现象;
(Ⅲ)与含碱的酚酞溶液共热,发现溶液中红色逐渐变浅以至无色。
根据上述现象,可以判断此混合物中一定含有 ,可能含有 ,一定没有 。(填结构简式)
(2)苯氯乙酮是一种具有荷花香味的有机物,其结构简式为:
请回答: 苯氯乙酮的同分异构体有多种,请写出同时符合下列三个条件的所有同分异构体的结构简式:
①分子内有苯环但不含甲基; ②氯原子与链烃基直接相连
③能发生银镜反应。。
(1)若 是某单烯烃与氢气加成后的产物,则烯烃可能有____种结构;若是炔烃与氢气加成的产物,则此炔烃可能有 种结构。
是某单烯烃与氢气加成后的产物,则烯烃可能有____种结构;若是炔烃与氢气加成的产物,则此炔烃可能有 种结构。
(2)已知某有机物的结构简式为:
①该有机物中所含官能团的名称是_______________________________。
②该有机物发生加成聚合反应后,所得产物的结构简式为_____ 。
③写出该有机物发生消去反应的化学方程式(注明反应条件):_________________________________。
(1)如图所示,烧杯甲中盛放100 mL 6 mol·L-1的HCl溶液,烧杯乙中盛放100 mL冷水,现向烧杯甲的溶液中放入NaOH固体,同时向烧杯乙中放入NH4NO3固体,搅拌使之溶解。A瓶中气体颜色变深,B瓶气体颜色变浅,理由是: 。
(2)在恒温条件下将一定量NO2和N2O4的混合气体通入一容积为2 L的密闭容器中,反应物浓度随时间变化关系如下图。
①图中的两条曲线,表示NO2浓度随时间的变化曲线
②前10 min内用υ(N2O4)表示的化学反应速率为
③25 min时,NO2转变为N2O4的反应速率增大,其原因是
④15min时的平衡常数为 ,35min时的平衡常数为 。
⑤在一定容积的密闭容器中,不能说明2NO2(g) N2O4(g)达到平衡状态的是()
N2O4(g)达到平衡状态的是()
| A.容器的压强不再变化 |
| B.容器的颜色不再变化 |
| C.混合气体的平均相对分子质量不再变化 |
| D.混合气体的密度不再变化 |
E.υ(NO2)=2υ(N2O4)
F.c(NO2)=2 c(N2O4)
请回答氯碱的如下问题:
(1)氯气、烧碱是电解食盐水时按照固定的比率k(质量比)生成的产品。理论上k=(要求计算表达式和结果);
(2)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。
①图中X.Y分别是、(填化学式),分析比较图示中氢氧化钠质量分数a%与b%的大小;
②分别写出燃料电池B中正极、负极上发生的电极反应
正极:;
负极:;