硫酸铜是一种重要的硫酸盐,在工农业生产中有着重要的应用。
回答下列问题:
(1)写出基态Cu2+的核外电子排布式 。
(2)SO42-中S原子的杂化轨道类型是 ;与SO42-互为等电子体的一种微粒是 。
(3) 胆矾CuSO4·5H2O可写成[Cu(H2O) 4]SO4·H2O,其结构示意图如下:
胆矾CuSO4·5H2O可写成[Cu(H2O) 4]SO4·H2O,其结构示意图如下:
①胆矾中含有的粒子间作用力是 (填序号)。
离子键 b.极性键 c.金属键 d.配位键 e.氢键 f.非极性键
②在硫酸铜溶液中加入过量KCN,生成配合物[Cu(CN)4]2-,指出1molCN-中 键的数目为 。
键的数目为 。
③胆矾受热分解得到铜的某种氧化物,其晶胞结构如图所示,则氧的配位数是 。
有可逆反应A(g)+B(g) 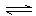 xC(g)+D(g),某温度时,在固定容积为2L的密闭容器内充入一定量的A、B,并保持温度不变。A、B、C、D物质的量随时间的变化如图所示:
xC(g)+D(g),某温度时,在固定容积为2L的密闭容器内充入一定量的A、B,并保持温度不变。A、B、C、D物质的量随时间的变化如图所示: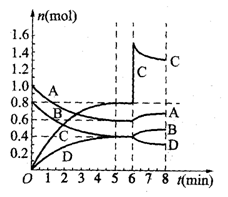
(1)根据图中所示,x=_______________;该反应的平衡状态为图中的____________min;
(2)0~5min的平均反应速率v(A)=_______________________________(用小数表示)。
(3)6min时改变影响平衡的一个条件,A、B、C、D的变化曲线如图中6~8min所示,则平衡_________移动(填“向左”、“向右”或“不”),可能的原因是________(选填序号)。
a、增大A的物质的量 b、加入催化剂
c、增加C的物质的量 d、减小容器体积
(4)若反应一开始就加入了合适的催化剂,在图中画出气体A在0~6min时的变化曲线。
某一反应体系中有反应物和生成物共6种:HC1、H2SO4、SnC12、SnC14、FeSO4、Fe2(SO4)3,反应前在溶液中滴加KSCN溶液显红色,反应后红色消失。
(1)该反应的氧化剂是。
(2)在该反应中,发生氧化反应的过程是→。
(3)写出并配平该反应的化学方程式,并标出电子转移的方向和数目:。
(4)SnC14与SnC12可用Hg2+来鉴别,HgC12与SnC12反应的产物是SnC14和Hg2C12(白色沉淀),该反应中还原剂与氧化剂的物质的量之比为。
四种短周期元素的性质或结构信息如下表。请根据信息回答下列问题。
| 元素 |
T |
X |
Y |
Z |
| 性质 结构 信息 |
人体内含量最多的元素,且其单质是常见的助燃剂。 |
单质为双原子分子,分子中含有3对共用电子对,常温下单质气体性质稳定,但其原子较活泼 |
单质质软、银白色固体、导电性强。 单质在空气中燃烧发出黄色的火焰。 |
第三周期元素的简单离子中半径最小 |
(1)写出元素T的离子结构示意图;写出元素X的气态氢化物的电子式;写出Z元素原子的原子结构示意图:;元素Y的最高价氧化物对应水化物的电子式______
(2)Z单质与Y最高价氧化物的水化物的水溶液反应的离子方程式
(3) 元素T与氟元素相比,非金属性较强的是(用元素符号表示),下列表述中能证明这一事实的是
a.常温下氟气的颜色比T单质的颜色深 b.氟气与T的氢化物剧烈反应,产生T的单质
c.氟与T形成的化合物中T元素呈正价态
d.比较两元素的单质与氢气化合时得电子的数目
有机物A可以通过不同的反应制得下列物质:
(1) 写出A → C的化学方程式:,
该反应类型为。
(2) 条件X是,推断B物质的结构简式为。
(3) 若E的结构中有两个六元环,则E的结构简式。
(4) R物质属于A 的同分异构体,其苯环上的一氯代物只有2种,性质如下:
试写出符合条件的R的结构简式。
CuSO4·5H2O是铜的重要化合物,有着广泛的应用。以下是CuSO4·5H2O的实验室制备流程图。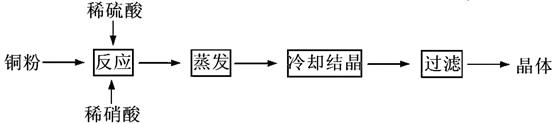
根据题意完成下列填空:
(1)理论上,为了制得纯净的CuSO4·5H2O晶体,需要消耗稀硫酸、稀硝酸溶质物质的量之比为,发生反应的离子方程式为。
(2)实际制得的胆矾晶体中还是含有一些杂质,通常采用法提纯。
(3)实际生产过程中对所加稀硝酸的浓度控制要求比较高,通常用标准氢氧化钠溶液来滴定。滴定过程中若用酚酞作指示剂,终点现象是 。请在右图中画出滴定过程中溶液的pH随所滴加氢氧化钠溶液体积的变化的曲线图(要求过A点)。
。请在右图中画出滴定过程中溶液的pH随所滴加氢氧化钠溶液体积的变化的曲线图(要求过A点)。
(4)上述使用的标准氢氧化钠溶液已经通过基准物质的标定。下列物质中通常可用来标定碱液的基准物质是。
| A.醋酸 | B.草酸 | C.苯甲酸 | D.苯酚 |