某元素的一价阴离子,核外有10个电子,质量数为19,则中子数为
| A.9 | B.10 | C.11 | D.12 |
标准状况下,将V L气体(摩尔质量为M g/mol)溶于0.2L水中,所得溶液的密度是a g/cm3,则此溶液的物质的量浓度(mol/L)为()
A.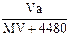 |
B.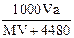 |
C.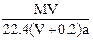 |
D.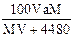 |
下列各步变化:A[HCl]→B[Cl2]→C[Ca(ClO)2]→D[HClO]→E[CO2],其中不能直接实现的是
| A.A→B | B.B→C | C.C→D | D.D→E |
下列除杂方案中,括号内为除去杂质所需的药品,其中正确的是
| A.NaOH溶液中混有Ba(OH)2 [K2SO4 ] | B.Cu(NO3)2溶液中混有AgNO3 [Cu粉] |
C.CO2中混有CO [炽热 的炭] 的炭] |
D.CO2中混有HCl气体[NaOH溶液] |
用10 mL的0.1 mol·L-1 BaCl2溶液恰好可使相同体积的硫酸铁、硫酸锌和硫酸钾三种溶液中的硫酸根离子完全转化为硫酸钡沉淀,则三种硫酸盐溶 液的物质的量浓度之比是C
液的物质的量浓度之比是C
| A.1:3:3 | B.1:2:3 | C.3:2:2 | D.3:1:1 |
下列物质在空气中久置会发生变质,且在变质过程中,既有氧化还原反应发生,又有非氧化还原反应发生的是
| A.苛性钠溶液 | B.漂白粉 | C.氯水 | D.生石灰 |