下列反应的离子方程式正确的是 ( )
| A.氯气通入氢氧化钠溶液中 Cl2 +2OH― = Cl― + ClO― + H2O |
| B.金属铁与稀硝酸反应 Fe + 2H+ = Fe2+ + H2↑ |
| C.在硅酸钠溶液中滴加稀硫酸 SiO32― + 2H+ = H2SO3↓ |
| D.铜粉与98.3%的硫酸加热下反应 Cu + 4H+ + SO42― = Cu2+ + SO2↑ + 2H2O |
下列有关化学用语正确的是()
| A.一CH3的电子式: | B. P原子的结构示意图; P原子的结构示意图; |
| C.醛基的结构简式:一COH | D.质量数为2的重氢原子: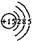 1 2H 1 2H |
在2010年上海世博会上,清洁能源、低碳经济、节能减排等理念得到了充分体现。下列做法中不能体现上述理念的是()
| A.供电系统引入以高纯硅为核心材料的光伏发电技术 |
| B.快餐饭盒用生物质材料“玉米塑料”(主要成分为聚乳酸)做成 |
| C.使用的卫生纸都是再生纸 |
| D.使用低合金高强钢作为建造中国馆的工程结构钢材 |
将100 mL稀硝酸和稀硫酸的混合酸溶液平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解9.6g(假设此时硝酸只被还原为NO,下同);向另一份中逐渐加入铁粉,产生气体的量随铁粉质量的变化如图所示。下列判断错误的是()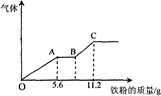
| A.OA段产生的气体是NO,BC段产生的气体是H2 |
| B.A点对应消耗NO3-物质的量为0.1 mol |
| C.B点对应的消耗铁粉的质量为8.4 g |
| D.原混合酸溶液中H2SO4浓度为2.0 mol·L-1 |
高铁电池是一种新型可充电电池,该电池能长时间保持稳定的放电电压。高铁电池的总反应为: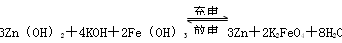 下列判断正确的是
下列判断正确的是
| A.充电时阳极反应为:2FeO42-+8H2O-6e-=2Fe(OH)3+10OH- |
| B.充电时阴极附近溶液的pH变大 |
| C.放电时,负极材料为Zn |
| D.放电时,每转移0.2 mol电子,正极的质量减少6.5 g |
有机物甲(结构如图所示)是合成西洛他唑(商品名platal)的重要中间体,也是合成抗血栓药、哮喘药、强心药等药的重要中间体。下列对它的分析合理的是()
| A.甲分子中可能所有原子共平面 |
| B.甲分子中没有手性碳原子 |
| C.甲的核磁共振氢谱图上有9种不同的峰 |
| D.1 mol甲最多可以分别和1 molNaOH、2 molBr2反应 |