短周期中的A、B、C、D、E五种元素,原子序数依次增大,A和D,C和E分别同主族,A为非金属元素,且A与B的原子序数之和等于C的原子序数,C2–与D+的核外电子数相等。则下列说法正确的是
A.B与A只能组成BA3化合物
B.第三周期中,D原子的原子半径最大
C.A、B、C三元素不可能形成离子化合物
D.E的氧化物对应的水化物一定有强的氧化性
下列说法正确的是
| A.金属阳离子都只有氧化性 |
| B.离子化合物都是强电解质 |
| C.金属与盐溶液的反应都是置换反应 |
| D.酸和碱发生的反应都属于复分解反应 |
某同学按下图所示的步骤配制50mL 一定物质的量浓度的NaOH溶液,其中不正确的操作有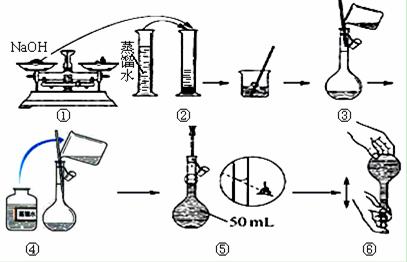

| A.②⑤ | B.①②⑤ | C.①②③⑤ | D.①②③④⑤ |
以下有关物质的质量分数和物质的量浓度的叙述正确的是
| A.等体积硫酸铁、硫酸铜、硫酸钾溶液分别与足量的氯化钡溶液反应,若生成硫酸钡沉淀的质量相等,则三种硫酸盐溶液的物质的量浓度之比为1:1:1 |
| B.Na2O2和Na2O各0.1mol分别放入100g水中,所得溶液的物质的量浓度不相等 |
| C.质量分数分别为5%和15%的氨水等体积混合后所得溶液的质量分数为10% |
D.20℃时,饱和KCl溶液的密度为1.174g•cm-3,物质的量浓度为4.0 mol•L-1,则此溶液中KCl的质量分数为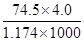 ×100% ×100% |
设NA为阿佛加德罗常数的数值,下列说法正确的是
| A.1 L 0.1mol•L-1Na2CO3溶液中有0.1NA个CO32- |
| B.常温常压下,22gCO2中共有2NA个共用电子对 |
| C.0.1mol Na2O2与水完全反应,转移的电子数为0.2NA |
| D.2.8gN2、CO和C2H4组成的混合气体所占有的体积约为2.24L |
下表为元素周期表前四周期的一部分,下列有关W、X、Y、Z四种元素的叙述中,正确的是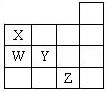
| A.与氢原子形成的化学键的键能:W比Y的大 |
| B.与氢原子形成的化学键的极性:X比Y的弱 |
| C.最低价气态氢化物的沸点:X的比W的高 |
| D.XZ3的晶体属于离子晶体 |