有一固体粉末,其中可能含有Na2CO3、NaCl、Na2SO4、CuCl2、Ba(NO3)2、K2CO3、K2SO4中的一种或几种,现按下列步骤进行实验。
(1)将该粉末溶于水得无色溶液和白色沉淀。
(2)在滤出的沉淀中加入过量稀硝酸,有部分沉淀溶解,同时产生无色气体。
(3)取滤液做焰色反应,火焰呈黄色,透过蓝色的钴玻璃观察,未见紫色火焰。由上述现象推断:该混合物中一定有 、 、
;一定不含有 、 、 ;
可能含有 。
乙烯、苯是重要的化工原料,请写出下列化学方程式及反应类型。
(1)一定条件下,乙烯与水反应的化学方程式
反应类型为
(2)在适当的温度、压强和有催化剂存在的条件下,乙烯可形成高分子化合物聚乙烯,该反应方程式为
反应类型为
(3)苯与液溴在催化剂条件下反应的化学方程式为
反应类型为
短周期元素ABCD原子序数依次增大。A元素原子核内无中子;B元素原子核外最外层电子数是次外层电子数的2倍;C元素是地壳含量最多的元素;D在短周期元素中金属性最强。请回答:
(1)B在元素周期表中的位置是。
(2)A与C可形成10电子分子,其化合物类型为(填“离子”或“共价”)化合物。
(3)A与C还可以形成一种18电子分子,向其溶液中加入少量二氧化锰粉末,反应的化学方程式为。
(4)D与C按原子个数比为1:1组成的化合物与BC 反应的化学方程式为
反应的化学方程式为
。
下表为元素周期表的一部分,针对表中的①~⑨九种元素,请回答有关问题: (1)⑨的元素符号是__________
(1)⑨的元素符号是__________
(2)在这些元素中,化学性质最不活泼的原子结构示意图为
(3)这些元素的最高价氧化物对应的水化物中,酸性最强的是(填化学式,下同),碱性最强的是,显两性的是。
(4)将元素①与氢元素组成的最简单有机物和⑥的单质按1:1混合后的气体在光照条件下放置一段时间,最多能得到产物。
(5)用电子式表示④和⑥两元素形成化合物的过程为。
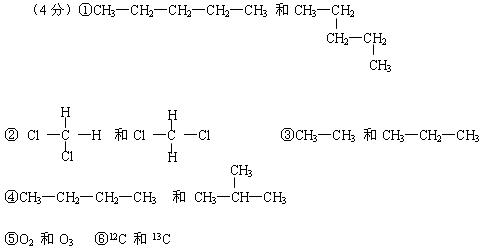
(1)组两原子互为同位素;(2)组是同一物质;
(3)组两物质互称为同系物;(4)组两物质互为同分异构体。
(6分)某温度时,在2L密闭容器中,X、Y、Z 三种物质的物质的量随时间变化的曲线如图所示。由图中数据分析:
(1)该反应的化学方程式:;
(2)反应开始至2min末,X的反应速率为(mol·L-1·min-1);
(3)3min后图中曲线所表示的含义是。