下列物质的应用或转化与氧化还原反应原理有关的是
| A.工业上煅烧石灰石制生石灰 |
| B.用明矾净用水 |
| C.稀盐酸除去钢铁表面的铁锈 |
| D.工业上用铁矿石炼铁 |
糖类、脂肪和蛋白质是维持人体生命活动所必需的三大营养物质,以下叙述正确的是
| A.淀粉、纤维素没有甜味,因此不属于糖类 |
| B.油脂属于酯类化合物,油脂的水解反应叫皂化反应 |
| C.葡萄糖能发生氧化反应和水解反应 |
| D.浓硝酸溅在皮肤上,使皮肤呈黄色是由于浓硝酸和蛋白质发生了颜色反应 |
一定温度下,反应N2(g)+3H2(g)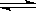 2NH3(g)达到化学平衡状态的标志是
2NH3(g)达到化学平衡状态的标志是
| A.N2、H2和NH3的浓度不再改变 |
| B.c(N2)∶c(H2)∶c(NH3)=1∶3∶2 |
| C.N2与H2的物质的量之和是NH3的物质的量2倍 |
| D.单位时间里每增加1molN2,同时增加3molH2 |
下列说法中正确的是
| A.用完的干电池可以随意地丢弃 |
| B.增加炼铁高炉的高度不可以降低尾气中CO的含量 |
| C.使用催化剂一定能加快化学反应速率 |
| D.把煤粉碎了再燃烧可以降低环境污染 |
实验室用下列两种方法制氯气:①用含HCl 146g的浓盐酸与足量的MnO2反应;②用87gMnO2与足量浓盐酸反应。所得的氯气
| A.①比②多 | B.②比①多 | C.一样多 | D.无法比较 |
已知:①能量越低的物质就越稳定,②白磷转化成红磷是放热反应。据此,下列判断或说法中正确的是
| A.在相同的条件下,红磷比白磷稳定 |
| B.在相同的条件下,白磷比红磷稳定 |
| C.红磷和白磷的结构相同 |
| D.红磷容易发生自燃而白磷则不会自燃 |