下列各溶液中,相关微粒物质的量浓度关系不正确的是
| A.0.1 mol·L-1NH3·H2O溶液中:c(NH4+)<c(OH-) |
| B.0.1 mol·L-1NH4C1溶液中:c(NH4+)+c(H+)==c(Cl-)+c(OH-) |
| C.0.1 mol·L-1Na2CO3溶液中:c((HCO3-)+c(CO3-)+c(H2CO3)="0.1" mol·L-1 |
| D.浓度均为0.1 mol·L-1的NH4Cl、CH3COONH4,NH4HSO4溶液,c(NH4+)大小顺序: |
CH3COONH4>NH4Cl>NH4HSO4
洋蓟素是一种新结构类型的抗乙型肝炎病毒和抗艾滋病病毒的化合物,其结构如下图所示,有关洋蓟素的说法正确的是(连四个不同基团的碳属于手性碳)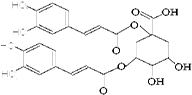
| A.分子中含有6个手性碳原子 |
| B.不能与氯化铁溶液发生显色反应 |
| C.一定条件下能发生酯化反应和消去反应 |
| D.1 mol洋蓟素最多可与11 mol NaOH反应 |
常温下,用0.1000 mol/L NaOH溶液分别滴定20. 00 mL 0.1000 mol/L 盐酸和20. 00 mL 0.1000 mol/L 醋酸溶液,得到2条滴定曲线,如下图所示。若以HA表示酸,下列说法正确的是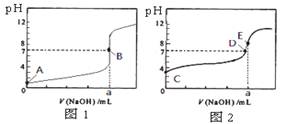
A.滴定盐酸的曲线是图2
B.达到B、D状态时,两溶液中离子浓度
均为c(Na+) = c(A—)
C.达到B、E状态时,反应消耗的n(CH3COOH)>n(HCl)
D.当0 mL< V(NaOH) <20. 00 mL时,对应混合溶液中各离子浓度由大到小的顺序均
为c(A—) >c(Na+)> c(H+) > c(OH—)
利用下列实验装置(依次为①—④)能完成相应实验的是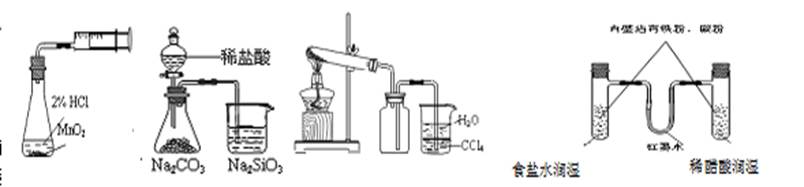
| A.实验①测定化学反应速率 | B.②能证明非金属性 Cl>C>Si |
| C.实验③室制取并收集NH3 | D.装置④模拟铁的腐蚀 |
下列离子方程式与所述事实相符且正确的是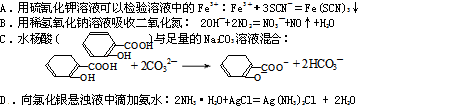
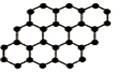
设NA表示阿伏加德罗常数的数值,下列说法不正确的是
| A.标况下,22.4LN2和NH3混合气体中原子间共有3NA个共用电子对 |
| B.3.0g甲醛和乙酸混合物中共含碳原子数为0.1NA |
| C.在1L0.1mol/L的HCOOH溶液中,所含HCOO-与HCOOH粒子数之和为0.1NA |
| D.12g石墨烯(厚度只有一个碳原子的单层石墨,结构如右图)中含有3NA个碳碳单键 |