下列描述错误的是( )
| A.可以使用排水法收集氨气 | B.Na2O2既含有离子键,又含有非极性键 |
| C.金属元素从游离态变为化合态一定被氧化 | D.Na2CO3饱和溶液中持续通入CO2气体有固体析出 |
下列离子方程式正确的是
| A.钠与水反应:2Na+2H2O ="===" 2Na++2OH-+H2↑ |
| B.氧化钠与盐酸反应:O2-+2H+="===" H2O |
C.CaCO3悬浊液中通CO2:CO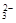 +CO2+H2O ="===" 2HCO +CO2+H2O ="===" 2HCO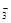 |
D.小苏打溶液与NaOH溶液混合:HCO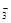 +OH-="===" CO +OH-="===" CO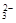 + H2O + H2O |
下列反应中,Na2O2只表现强氧化性的是
| A.2Na2O2 + 2CO2 |
| B.Na2O2 + MnO2 = Na2MnO4 |
C.5Na2O2 + 2MnO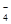 + 16H+ = 10Na+ + 2Mn2+ + 5O2↑ + 8H2O + 16H+ = 10Na+ + 2Mn2+ + 5O2↑ + 8H2O |
| D.2Na2O2 + 2H2SO4 = 2Na2SO4 +2H2O + O2↑ |
关于铷及其化合物的性质的推测正确的是
| A.铷跟冷水反应比钾更剧烈,但不能置换出CuSO4溶液中的Cu单质 |
| B.铷的熔点比钠高 |
| C.Rb2CO3受热易分解,生成Rb2O和CO2 |
| D.铷在氧气中燃烧生成Rb2O |
已知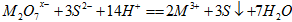 中的M的化合价为
中的M的化合价为
| A.+2 | B.+3 | C.+4 | D.+6 |
将一定量的CO2通入下列溶液中,一定变浑浊的是
| A.CaCl2溶液 | B.澄清石灰水 |
| C.饱和Na2CO3溶液 | D.稀H2SO4 |