在1 L密闭容器中发生反应:4NH3(g)+5O2(g) 4NO(g)+6H2O(g)
4NO(g)+6H2O(g)
△H=-Q kJ·mol-1(Q>O),容器内部分物质的物质的量浓度如下表:
| 时间/浓度 |
c(NH3) (mol/L) |
c(O2 ) (mol/L) |
c(NO) (mol/L) |
| 起始 |
0.8 |
1.6 |
0 |
| 第2min |
0.6 |
a |
0.2 |
| 第4min |
0.3 |
0.975 |
0.5 |
| 第6min |
0.3 |
0.975 |
0.5 |
| 第8min |
0.7 |
1.475 |
0.1 |
| 第10min |
0.7 |
1.475 |
0.1 |
下列说法错误的是
A.反应在第2 min到第4min时,O2的平均反应速率为0.1875 mol/(L·min)
B.反应在第2 min时改变了某一条件,该条件可能是使用催化剂或升高温度
C.第4 min时、第8 min时分别达到化学平衡,且平衡常数不相同
D.在开始反应的前2 min内,该反应的△H=-0.05Q kJ·mol-1
下列依据相关实验得出的结论正确的是
| A.加入硫酸铜可使锌与稀硫酸的反应速率加快,说明Cu2+具有催化作用 |
| B.纤维素的水解产物能够发生银镜反应,说明纤维素是一种还原性糖 |
| C.向某溶液中滴加硝酸酸化的Ba(NO3)2溶液产生白色沉淀,说明该溶液中含有SO42- |
| D.等物质的量浓度的H3PO4溶液的pH比H2SO4溶液大,说明硫比磷的非金属性强 |
新型纤维酸类降脂药克利贝特可由物质X在一定条件下反应制得:
下列有关叙述正确的是
| A.克利贝特的分子式为C28H36O6 |
| B.物质X分子中所有碳原子可能位于同一平面内 |
| C.1 mol物质X最多可以与含2 molBr2的溴水反应 |
| D.用饱和NaHCO3溶液可以鉴别物质X和克利贝特 |
下列有关说法正确的是
| A.因为合金在潮湿的空气中易形成原电池,所以合金耐腐蚀性都较差 |
| B.合成氨的反应是放热反应,则采用低温条件可以提高氨的生成速率 |
| C.常温下2S2O(g)=3S(s)+SO2(g)能自发进行,可推断该反应为放热反应 |
| D.NH4Cl和HCl溶于水后滴加石蕊都变红色,说明它们均能电离出H+ |
短周期元素原子序数之和为28,X+与Z2-具有相同的核外电子层结构,Y、Z在同一周期。下列推测正确的是
| A.元素Y的最高化合价为+7 |
| B.三种元素的原子半径rZ>rY>rX |
| C.Z的单质比Y的单质更易与H2反应 |
| D.化合物X2Z2中阴阳离子数之比为1: 2 |
锌溴液流电池是一种新型电化学储能装置(如图所示),电解液为溴化锌水溶液,电解液在电解质储罐和电池间不断循环。下列说法不正确的是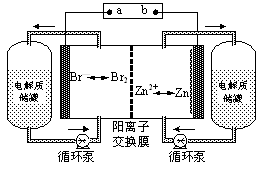
| A.充电时电极a连接电源的负极 |
| B.放电时负极的电极反应式为Zn—2e-=Zn2+ |
| C.放电时左侧电解质储罐中的离子总浓度增大 |
| D.阳离子交换膜可阻止Br2与Zn直接发生反应 |