为了证明CO具有还原性,有人利用下列装置设计了系列的实验,其中A为气体发生装置,C为尾气处理装置,X装置可以盛放不同的试剂重复使用。已知草酸与浓硫酸共热发生如下反应: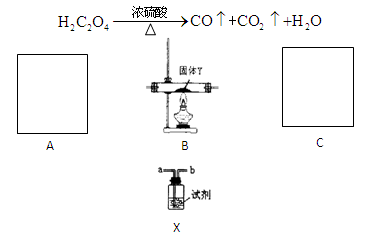
(1)若以草酸.浓硫酸为原料制备一氧化碳,则该气体发生装置中所用到的玻璃仪器除了
导管、分液漏斗外,还有______________________________。
(2)装置连接无误,装入药品后,在加热装置B之前应进行的一步操作是__________,C中尾气的的处理方法是______________________________。
(3)已知B中固体为CuO,现要制得纯净干燥的CO以验证其还原性,则A.B之间放置的X装置(可重复)中所装试剂依次为:____________________,澄清石灰水,____________________,证明CO具有还原性的现象为____________________。
(4)除上述现象外,若再用一次X装置,还有一种能说明CO具有还原性的现象,
则装置X的安装位置及所装试剂为:______________,现象为:___________________。
苯甲酸及其钠盐可用作乳胶、牙膏、果酱或其它食品的抑菌剂,也可广泛应用于制药和化工行业,某同学尝试用甲苯的氧化反应制备苯甲酸,制备流程为:
操作步骤如下:① 将一定量的甲苯和碱性KMnO4溶液加热至沸腾,并冷凝回流至混合液不再分层。② 反应停止后,将反应混合液过滤,滤渣为黑色固体;得到的滤液如果呈紫色,可加入少量的饱和亚硫酸钠溶液使紫色褪去,重新过滤。③ 将②中所得滤液经一系列操作得到苯甲酸晶体。
已知:苯甲酸相对分子质量122,熔点122.4℃,在25℃和95℃时溶解度分别为0.3g和6.9g;
(1)该实验合成苯甲酸钾可能用到的下列仪器有__________。
A.圆底烧瓶B.蒸馏烧瓶 C.冷凝管D.温度计
(2)第①步中被回流的主要物质是____________________。
(3)写出滴加饱和亚硫酸钠溶液时的离子方程式______________________________。
(4)步骤③得到苯甲酸晶体应进行操作是________(按操作顺序填正确答案序号)。
A.酸化 B.过滤 C.蒸发浓缩D.冷却结晶
实验室中,用硫铁矿烧渣(主要成分为Fe2O3、FeO、SiO2等)为原料制备高纯氧化铁(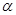 —
—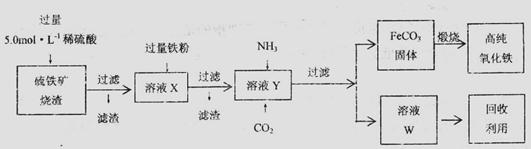
Fe2O3)的步骤如下:
回答下列问题:
(1)上述实验中,加入铁粉的作用是____________。(用离子方程式表示)实验中检验溶液x中的离子是否与铁粉完全反应的试剂是____________溶液
(2)实验室欲用18.4 mol·L-1。的浓硫酸配制100 mL5.0mol·L-1的硫酸溶液,所用仪器除胶头滴管、量筒、烧杯、玻璃棒外,还有_________(填写仪器名称);
(3)某同学用下图所示装置实现向溶液Y中通入NH3和CO2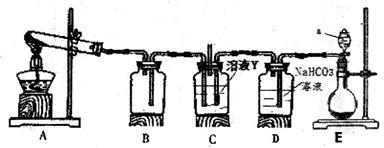
①上述装置的中,仪器a的名称是_______;装置B的作用是____________________。
②圆底烧瓶内放置的固体药品为________(填化学式);试管内发生反应的化学方程式为_________________。
③甲、乙、丙三位同学分别用上述装置进行实验,装置C的试剂瓶内溶液体积相等。
若甲、乙两同学实验中,通入的NH3和CO2的物质的量之比分别为2:l和l:l,恰好完全反应后,溶液中水的电离程度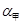 ________(填“>”“=”或“<”)
________(填“>”“=”或“<”)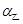 。
。
若丙同学未用装置D,则反应后溶液中离子浓度间的关系为[H+]+[NH4+]=_______。
(12分)金属单质及其化合物在生产生活中应用非常广泛,废旧金属的回收利用是重要研究课题。某学习小组在实验室中模拟利用含铜废料(主要成分为Cu和CuO,还有少量的A1,Fe及其氧化物)生产胆矾,其实验方案如下:
(1)上述流程中,操作1所得“滤液’‘的主要成分为_____________;
(2)酸溶后所得溶液中的榕质主要有_____________;
(3)请写出酸溶过程单质铜发生反应的离子方程式___________;该反应中氧化剂与还原剂的物质的量之比为______________;
(4)试剂可以是________________;
(5)操作3是一系列操作.其操作为______________、冷却结晶、过滤、___________、小心干燥。
(12分)氯气是一种重要的工业原料。
(1)实验室可用高锰酸钾和浓盐酸反应制取氯气,反应的化学方程式是:__________________。
(2)资料显示:
某学习小组利用此原理设计如图所示装置制取氯气并探究其性质。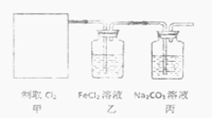
①在该实验中,甲部分的装置是______(填字母)。如何检查该装置的气密性?_________________。
②乙装置中FeCl2溶液与Cl2反应的离子方程式是_______________。
③丙装置中通入少量Cl2,可制得某种生活中常用的漂白、消毒的物质。已知碳酸的酸性强于次氯酸。则丙中发生反应的化学方程式是____________。
④该实验存在明显的缺陷.改进的方法是_______________________________________________。
下表是实验室制备气体的有关内容:
| 编号 |
实验内容 |
实验原理 |
气体发生装置 |
| ① |
制备氧气 |
H2O2→O2 |
|
| ② |
制备氨气 |
NH4Cl→NH3 |
|
| ③ |
制备氯气 |
HCl→Cl2 |
(1)从上述气体制备原理中:从制备过程看,必须选择合适的氧化剂才能实现的是(填气体的化学式,下同);从反应原理看,明显不同于其他两种气体的是。
(2)根据表中所列实验原理,从下列装置中选择合适的气体发生装置,将其编号填入上表中的空格中。
(3)某学习小组设计了如下图实验,将氯气依次通过下列装置以验证氯气的性质: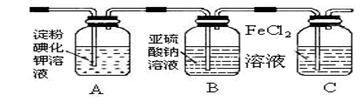
①通入氯气后,A中的现象是,
整套实验装置存在的明显缺陷是。
②C装置中发生反应的离子方程式为:。