X、Y、Z、W为四种短周期元素,它们在周期表中位于连续的四个主族,如图所示。Z元素原子核外K层与M层电子数相等。下列说法中正确的是( )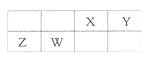
| A.Y元素最高价氧化物对应的水化物化学式为H3YO4 |
| B.Y最简单气态氢化物的水溶液显弱碱性 |
| C.原子半径由小到大的顺序为:X<Z<Y<W |
| D.X、Z两种元素的氧化物中所含化学键类型相同 |
若两物质恰好完全反应,下列各项中反应前后保持不变的是
①电子总数;②原子总数;③分子总数;④物质的总能量;⑤物质的总质量
| A.①②⑤ | B.①③⑤ | C.②③④ | D.②④⑤ |
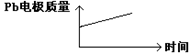
为增强铝的耐腐蚀性,现以铅蓄电池为外电源,以A1作阳极、Pb作阴极,电解稀硫酸,使铝表面的氧化膜增厚。反应原理如下:电池:Pb(s)+ PbO2(s)+2H2SO4(aq)= 2PbSO4(s)+ 2H2O(l)
电解池:2Al + 3H2O  Al2O3 + 3H2↑,电解过程中,以下判断正确的是( )
Al2O3 + 3H2↑,电解过程中,以下判断正确的是( )
| 原电池 |
电解池 |
|
| A |
H+移向Pb电极 |
H+移向Pb电极 |
| B |
每消耗3molPb |
生成2molAl2O3 |
| C |
正极:PbO2+4H++2e-=Pb2++2H2O |
阳极:2Al+3H2O-6e-=Al2O3+6H+ |
| D |
 |
 |
下表所列各组第Ⅰ栏中的化学反应与第Ⅱ栏中的化学反应,都可以用第Ⅲ栏中的离子方程式表示的是
| 选项 |
第Ⅰ栏 |
第Ⅱ栏 |
第Ⅲ栏 |
| A |
往少量NaOH溶液中投入铝片 |
往过量NaOH溶液中投入铝片 |
2Al+2OH-+2H2O=2AlO2-+3H2↑ |
| B |
往Fe2(SO4)3溶液中滴入氢氧化钠溶液 |
往Fe2(SO4)3溶液中滴入氢氧化钡溶液 |
Fe3++3OH-=Fe(OH3)↓ |
| C |
往NaHCO3溶液中滴入Ca(OH)2溶液 |
往NaHCO3溶液中滴入NaOH溶液 |
OH-+HCO3-=CO32-+H2O |
| D |
往NaOH溶液中通入过量CO2气体 |
往NaOH溶液中通入少量CO2气体 |
CO2+OH-=HCO3- |
根据下列实验现象,所得结论正确的是
A B C D
| 实验 |
实验现象 |
结论 |
| A |
左烧杯中铁表面有气泡,右边烧杯中铜表面有气泡 |
活动性:Al>Fe>Cu |
| B |
左边棉球变为橙色,右边棉球变为蓝色 |
氧化性:Cl2>Br2>I2 |
| C |
先生成蓝色沉淀,后产生白色沉淀 |
溶度积常数:Mg(OH)2<Cu(OH)2 Cu(OH)2Mg(OH)2<Cu(OH)2MgMg(OH)2<Cu(OH)2Mg(OH)2<Cu(OH)2 |
| D |
锥形瓶中有气体产生,烧杯中液体变浑浊 |
非金属性:Cl>C>Si |
25℃时,用浓度为0.1000 mol/L的NaOH溶液滴定20.00 mL浓度均为0.1000 mol/L的三种酸HX、HY、HZ,滴定曲线如图所示。下列说法正确的是( )
| A.在相同温度下,同浓度的三种酸溶液的导电能力顺序: HZ<HY< HX |
| B.在HZ中加入NaOH至恰好完全反应时,溶液中各离子浓度大小顺序: c(Na+)>c(Z-)>c(OH—)>c(H+) |
| C.将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时:c(X—)+c(Y—)+c(OH—)= c(Na+)+c(H+) |
| D.将HX和HZ溶液混合后,用NaOH溶液滴定至HX恰好完全反应时:c(Na+)= c(X—)+ c(Z—) |