下列说法错误的是( )
| A.胶体有吸附性 |
| B.将FeCl3稀溶液溶于冷水即可制得Fe(OH)3胶体 |
| C.胶体的分散质颗粒可以透过滤纸 |
| D.分散系中分散质粒子直径由大到小的顺序是:浊液、胶体、溶液 |
下列说法正确的是( )
| A.油脂在酸性或碱性条件下均可发生水解反应,且产物相同 |
| B.用核磁共振氢谱不能区分HCOOCH3和HCOOCH2CH3 |
| C.用Na2CO3溶液不能区分CH3COOH和CH3COOCH2CH3 |
| D.室温下,在水中的溶解度:丙三醇>苯酚>1氯丁烷 |
在过量的稀硫酸溶液中加入5.6g铁粉,待反应完全后,再加入50 mL 0.5mol·L-1 KNO3溶液,恰好反应完全。该反应的方程式为:__FeSO4+__KNO3+__H2SO4===__K2SO4+__Fe2(SO4)3+__NxOy+__H2O,则对该反应的下列说法正确的是( )。
| A.反应中还原产物是NO |
| B.化学方程式中按物质顺序的计量数是:8、2、5、1、4、1、5 |
| C.反应过程中转移的电子数为8e- |
| D.氧化产物和还原产物的物质的量之比为1∶4 |
在200 mL某硫酸盐溶液中含有1.5NA个硫酸根离子(NA表示阿伏加德罗常数),同时含有NA个金属阳离子,则该硫酸盐的物质的量浓度为( )
| A.1 mol/L | B.2 mol/L | C.2.5 mol/L | D.5 mol/L |
在t ℃时,将a g NH3完全溶于水,得到V mL溶液,设该溶液的密度为ρ g·cm3,质量分数为w,其中含NH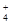 的物质的量为b mol。下列叙述中不正确的( )。
的物质的量为b mol。下列叙述中不正确的( )。
A.溶质的质量分数w= ×100% ×100% |
B.溶质的物质的量浓度c=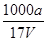 mol·L-1 mol·L-1 |
C.溶液中c(OH-)=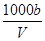 mol·L-1+c(H+) mol·L-1+c(H+) |
| D.上述溶液中再加入V mL水后,所得溶液中溶质的质量分数小于0.5 w |
使用容量瓶配制溶液时,由于操作不当,会引起误差,下列情况会使所配溶液浓度偏低的是
①用天平(使用游码)称量时,被称量物与砝码的位置放颠倒了 ②用滴定管量取液体时,开始时平视读数,结束时俯视读数 ③溶液转移到容量瓶后,烧杯及玻璃棒未用蒸馏水洗涤 ④转移溶液前容量瓶内有少量蒸馏水 ⑤定容时,仰视容量瓶的刻度线 ⑥定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线
| A.①②⑤⑥ | B.①③⑤⑥ | C.②③④⑥ | D.③④⑤⑥ |