已知:2H2(g)+O2(g)===2H2O(l) ΔH=-571.6 kJ/mol,下列叙述正确的是
| A.是指常温常压下,2个氢分子和1个氧分子反应生成2个水分子,放出热量571.6 kJ |
| B.是指常温常压下,2 mol H2(g)和1 mol O2(g)反应生成2 mol H2O(l),放出热量571.6 kJ |
| C.是指标准状况下,2 mol H2O(l)分解为2 mol H2(g)和1 mol O2(g),吸收热量571.6 kJ |
| D.是指常温常压下,2 mol H2(g)和1 mol O2(g)反应生成2 mol H2O(g),放出热量571.6 kJ |
向m g镁和铝的混合物中加入适量的稀硫酸,恰好完全反应生成标准状况下的气体b L。向反应后的溶液中加入c mol/L氢氧化钾溶液V mL,使金属离子刚好沉淀完全,得到的沉淀质量为n g。再将得到的沉淀灼烧至质量不再改变为止,得到固体p g。则下列关系不正确的是
A.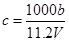 |
B.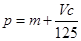 |
C.n=m+17Vc | D.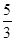 m<p< m<p< |
25 ℃,101 k Pa时,强酸与强碱的稀溶液发生中和反应的中和热为57.3 kJ/mol,辛烷的燃烧热为5518 kJ/mol。下列热化学方程式书写正确的是 ( )
A.2H+(aq)+SO42-(aq)+Ba2+(aq)+2OH-(aq)=BaSO4(s)+2H2O(1)△H=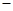 57.3 kJ/mol 57.3 kJ/mol |
B.KOH(aq)+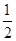 H2 SO4(aq)= H2 SO4(aq)=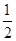 K2SO4(aq)+H2O(l)△H= K2SO4(aq)+H2O(l)△H=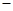 57.3kJ/mol 57.3kJ/mol |
C.C8H18(I)+ O2(g)=8CO2(g)+9H2O△H= O2(g)=8CO2(g)+9H2O△H=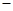 5518 kJ/mol 5518 kJ/mol |
D.2C8H18(g)+25O2(g)=16CO2(g)+18H2O(1)△H=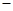 5518 kJ/mol 5518 kJ/mol |
25°C时,几种弱酸溶液的PH如下表所示:
| 弱酸 |
CH3COOH |
H2SO3 |
HCN |
| 物质的量浓度mol/L |
0.01 |
0.01 |
0.01 |
| PH |
3.4 |
2.3 |
5.6 |
下列有关说法正确的是
A.相同PH的CH3COOH与HCN溶液中水电离的氢离子浓度CH3COOH溶液中的大
B.物质的量浓度相同的CH3COONa与NaCN溶液中,各离子浓度之和两者相等。
C.25°C时,HCN溶液的电离平衡常数(Ka)与NaCN溶液的水解平衡常数(K)存在
如下关系:Ka ·K = Kw
D.0.01mol/L的Na2SO3溶液与0.01mol/L的CH3COONa溶液相比,一定是后者的碱性强
已知SO32-+I2+H2O=SO42-+2I-+2H+。某溶液中可能含有I-、NH4+、Cu2+、SO32-,向该无色溶液中加入少量溴水,溶液仍呈无色。则下列关于该溶液组成的判断正确的是
| A.肯定不含I- | B.肯定不含Cu2+ | C.可能含有SO32- | D.肯定不含有NH4+ |
下列离子或分子组中能大量共存,且满足相应要求的是
| 选项 |
离子 |
要求 |
| A |
K+、NO3-、Cl-、HS- |
c(K+)<c(Cl-) |
| B |
Fe3+、NO3-、SO32-、Cl- |
逐滴滴加盐酸立即有气体产生 |
| C |
Na+、HCO3-、Mg2+、SO42- |
逐滴滴加氨水立即有沉淀产生 |
| D |
NH4+、Al3+、SO42-、CH3COOH |
滴加NaOH浓溶液立刻有气体产生 |