(16分,每空2分)已知非金属单质硫(S)是淡黄色固体粉末,难溶于水。为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题: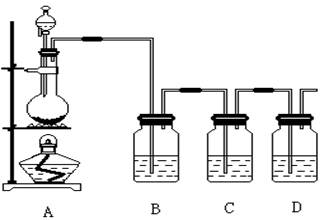
(1)装置A的分液漏斗中盛装的试剂是 ,烧瓶中的化学反应方程式 。
(2)装置B所加试剂饱和NaCl溶液,其装置的作用是 。
(3)装置C中盛放的试剂是 (选填下列所给试剂的代码),实验现象为 ,
该反应的离子方程式是 。
A.Na2S溶液 B.Na2SO3溶液 C.Na2SO4溶液
(4)已知:①硫酸比次氯酸稳定;②高氯酸比硫酸酸性强;③S2-比Cl-易被氧化;④HCl比H2S稳定;⑤铜与盐酸不反应,但能与浓硫酸反应;⑥铁与氯气加热生成三氯化铁,铁与硫加热生成硫化亚铁;⑦硫原子与氯原子电子层数相同,氯原子半径小于硫原子。可说明氯比硫非金属性强的是
A.全部 B.②③④⑥⑦ C.①②④⑤⑥ D.除 ①以外
(5)装置D中盛放烧碱溶液,目的是吸收反应后剩余的气体,防止污染空气,写出反应的离子方程式 。
金刚烷是一种重要的化工原料,工业上可通过下列途径制备:
请回答下列问题:
(1)环戊二烯分子中最多有个原子共平面:
(2)金刚烷的分子式为,其分子中的
:基团有个;
(3)下面是以环戊烷为原料制备环戊二烯的合成路线:
其中,反应①的产物名称是,反应②的反应试剂和反应条件是,反应③的反应类型是;
(4)已知烯烃能发生如下反应:
请写出下列反应产物的 结构简式:
结构简式:

(5) 是二聚环戊二烯的同分异构体,能使溴的四氯化碳溶液褪色, 经高锰酸钾酸性溶液加热氧化可以得到对苯二甲酸[提示:苯环上的烷基( , , )或烯基侧链经高锰酸钾酸性溶液氧化得羧基],写出 所有可能的结构简式(不考虑立体异构):
请回答下列实验室中制取气体的有关问题。
( 1)下图是用
与浓盐酸反应制取适量氯气的简易装置。
1)下图是用
与浓盐酸反应制取适量氯气的简易装置。
装置
、
、
的作用分别是:
;
;
.
(2)在实验室欲制取适量
气体。
①下图中最适合完成该实验的简易装置是(填序号);
②根据所选的装置完成下表(不需要的可不填)
|
应加入的物质 |
所起的作用 |
|
|
A |
||
|
B |
||
|
C |
||
|
D |
。
③简单描述应观察到的实验现象。
工业废水中常含有一定量的
和
,它们会对人类及生态系统产生很大的伤害,必须进行处理。常用的处理方法有两种。
方法1:还原沉淀法
该法的工艺流程为
其中第①步存在平衡:
(1)若平衡体系的
,则溶液显色.
(2)能说明第①步反应达平衡状态的是。
a.
和
的浓度相同
b.
c.溶液的颜色不变
(3)第②步中,还原1mol
离子,需要mol的
。
(4)第③步生成的
在溶液中存在以下沉淀溶解平衡:
常温下, 的溶度积 ,要使 降至 ,溶液的 应调至。
方法2:电解法
该法用
做电极电解含
的酸性废水,随着电解进行,在阴极附近溶液
升高,产生
沉淀。
(5)用
做电极的原因为。
(6)在阴极附近溶液
升高的原因是(用电极反应解释)。
溶液中同时生成的沉淀还有。
某研究性学习小组为合成1-丁醇,查阅资料得知一条合成路线:

 ;
;
的制备原理:
 ↑+
,并设计出原料气的制备装置(如图)
↑+
,并设计出原料气的制备装置(如图)

请填写下列空白:
(1)实验室现有锌粒、稀硝酸、稀盐酸、浓硫酸、2-丙醇,从中选择合适的试剂制备氦气,丙烯。写出化学方程式:,。
(2)若用以上装置制备干燥纯净的
,装置中
和
的作用分别是,;
和
中承装的试剂分别是,。若用以上装置制备
, 气体发生装置中必需的玻璃仪器名称是 ;在虚线框内画出收集
干燥的装置图。
(3)制丙烯时,还产生少量
,
及水蒸气,该小组用以下试剂检验这四种气体,混合气体通过试剂的顺序是(填序号)
①饱和
溶液②酸性
溶液③石灰水
④无水
⑤品红溶液
(4)合成正丁醛的反应为正向放热的可逆反应,为增大反应速率和提高原料气的转化率,你认为应该采用的适宜反应条件是
a. 低温、高压、催化剂 b. 适当的温度、高压、催化剂
c. 常温、常压、催化剂 d. 适当的温度、常压、催化剂
(5)正丁醛经催化剂加氢得到含少量正丁醛的1-丁醇粗品,为纯化10-丁醇,该小组查阅文献得知:①
(饱和)→
↓;②沸点:乙醚34°C,1-丁醇118°C,并设计出如下提纯路线:
粗品 滤液
滤液
 有机层
有机层 1
1 丁醇、乙醚
丁醇、乙醚 纯品
纯品
试剂1为,操作1为,操作2为,操作3为_。
某同学进行实验研究时,欲配制
溶液,但只找到在空气中暴露已久的
试剂(化学式量:315)。在室温下配制溶液时发现所取试剂在水中仅部分溶解,烧杯中存在大量未溶物。为探究原因,该同学查得
在283
、293
和303
时的溶解度(
/100g H2O)分别为2.5、3.9和5.6。
(1)烧杯中未溶物仅为
,理由是
(2)假设试剂由大量
和少量
组成,设计实验方案,进行成分检验。在答题卡上写出实验步骤、预期现象和结论。(不考虑结晶水的检验;室温时
饱和溶液的
=9.6)
限选试剂及仪器:稀盐酸、稀硫酸、
溶液、澄清石灰水、pH计、烧杯、试管、带塞导气管、滴管
| 实验步骤 | 预期现象和结论 |
 步骤1:取适量试剂于洁净烧杯中,加入足量蒸馏水,充分搅拌,静置,过滤,得滤液和沉淀。 步骤1:取适量试剂于洁净烧杯中,加入足量蒸馏水,充分搅拌,静置,过滤,得滤液和沉淀。 |
|
| 步骤2:取适量滤液于试管中,滴加稀硫酸。 | |
| 步骤3:取适量步骤1中的沉淀于试管中,。 | |
| 步骤4: |
(3)将试剂初步提纯后,准确测定其中
的含量。实验如下:
①配制250
约
溶液:准确称取
克试样,置于烧杯中,加适量蒸馏水,,将溶液转入,洗涤,定容,摇匀。
②滴定:准确量取25.00
所配制
溶液于锥形瓶中,滴加指示剂,将(填"0.020"、"0.05"、"0.1980"或"1.5")
盐酸装入50
酸式滴定管,滴定至终点,记录数据。重复滴定2次。平均消耗盐酸
。
③ 计算
的质量分数=(只列出算式,不做运算)
(4)室温下,(填"能"或"不能") 配制
溶液。