下列各组热化学方程式中,化学反应的ΔH前者大于后者的是( )
①C(s)+O2(g)===CO2(g) ΔH1 C(s)+1/2O2(g)===CO(g) ΔH2
②S(s)+O2(g)===SO2(g) ΔH3 S(g)+O2(g)===SO2(g) ΔH4
③H2(g)+1/2O2(g)===H2O(l) ΔH5 2H2(g)+O2(g)===2H2O(l) ΔH6
④CaCO3(s)===CaO(s)+CO2(g) ΔH7 CaO(s)+H2O(l)===Ca(OH)2(s) ΔH8
| A.① | B.④ | C.②③④ | D.①②③ |
常温下,纯水中存在电离平衡:H2O H++OH-。欲使水的电离平衡向正方向移动,并使c(OH-)增大,应加入的物质是
H++OH-。欲使水的电离平衡向正方向移动,并使c(OH-)增大,应加入的物质是
| A.H2SO4 | B.AlCl3 | C.NaHCO3 | D.NaOH |
下列说法正确的是
| A.水解反应是吸热反应 | B.升高温度可以抑制盐类的水解 |
| C.正盐水溶液的pH均为7 | D.酸式盐的pH均小于7 |
下列离子方程式中属于水解反应的是
A.Cl2+H2O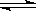 H++Cl-+HClO H++Cl-+HClO |
B.HS—+OH—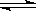 S2—+H2O S2—+H2O |
C.HCO3—+H2O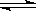 H3O++CO32— H3O++CO32— |
D.NH4++H2O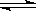 NH3·H2O+H+ NH3·H2O+H+ |
已知:H2(g)+F2(g)="2HF(g)" △H=-270kJ/mol,下列说法正确的是
| A.2L氟化氢气体分解成1L氢气与1L氟气吸收270kJ热量 |
| B.1mol氢气与1mol氟气反应生成2mol液态氟化氢放出热量小于270kJ |
| C.在相同条件下,1mol氢气与1mol氟气的能量总和大于2mol氟化氢气体的能量 |
| D.1个氢气分子与1个氟气分子反应生成2个氟化氢气体分子放出270热量 |
在石灰乳中存在平衡体系:Ca(OH)2(s)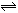 Ca2+(aq)+2OH-(aq),下列方法中,能使c(Ca2+)减小、c(OH-)增大的是
Ca2+(aq)+2OH-(aq),下列方法中,能使c(Ca2+)减小、c(OH-)增大的是
| A.加入少量MgCl2固体 | B.加入少量Na2CO3固体 |
| C.加入少量KCl固体 | D.加入少量CaO固体 |