以硫酸铜溶液作电解液,对含有杂质Fe、Zn、Ag的粗铜进行电解精炼。下列叙述正确的是
①粗铜与直流电源负极相连 ②阴极发生的反应为Cu2+ + 2e-= Cu
③电路中每通过3.01×1023个电子,得到的精铜质量为16 g
④杂质Ag以Ag2SO4的形式沉入电解槽形成“阳极泥”
| A.②③ | B.②④ | C.③④ | D.①③ |
下列物质中既含有非极性键,又含有离子键的是
| A.MgBr2 | B.H2O2 | C.Na2O2 | D.NH4Cl |
下列离子方程式书写正确的是
| A.少量CO2通入Ba(OH)2溶液中:CO2+2OH—= CO32— +H2O |
| B.NH4Al(SO4)2溶液中滴入Ba(OH)2溶液至SO42—恰好沉淀完全 NH4++Al3++2SO42—+2Ba2++4OH—= NH3·H2O+Al(OH)3↓+2BaSO4↓ |
| C.FeCl3溶液腐蚀铜线路板:Fe3++Cu = Fe2++Cu2+ |
| D.向NaHCO3溶液中滴入少量Ca(OH)2溶液:HCO3—+OH—= CO32—+H2O |
关于12C、14C、13N、14N几种原子的相互关系描述正确的是
A.14C和14N质量数相同,互为同位素
B.12C和14N含有相同的中子数
C.12C和 13N中子数相同,质子数不同,互为同位素
D.12CO和14CO物理性质不同,化学性质基本相同
下列说法中,正确的是
| A.第ⅠA族元素都比第ⅡA族元素金属性强 |
| B.只含有非金属元素的化合物可能是离子化合物 |
| C.只含有共价键的物质一定是共价化合物 |
| D.同主族元素原子半径越小越容易失去电子 |
下列化学用语表示正确的是
| A.原子核中有6个中子的硼原子:6 B | B.HCl的电子式: |
C.K+结构示意图: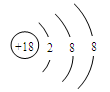 |
D.HClO的结构式:H—O—Cl |