(1)化合物A(C4H10O)是一种有机溶剂。A可以发生以下变化: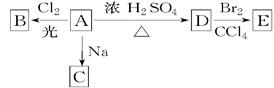
①A分子中的官能团名称是 ;
②A只有一种一氯取代物B。写出由A转化为B的化学方程式
;
③A的同分异构体F也可以有框图内A的各种变化,且F的一氯取代物有三种。F的结构简式是 。
(2)化合物“HQ”(C6H6O2)可用作显影剂,“HQ”可以与氯化铁溶液发生显色反应。“HQ”还能发生的反应是(选填序号) 。
①加成反应 ②氧化反应 ③加聚反应 ④水解反应
“HQ”的一硝基取代物只有一种。“HQ”的结构简式是 。
(3)A与“HQ”在一定条件下相互作用形成水与一种食品抗氧化剂“TBHQ”。“TBHQ”与氢氧化钠溶液作用得到化学式为C10H12O2Na2的化合物。
“TBHQ”的结构简式是 。
(1)元素
的离子与
所含电子数和质子数均相同,则
的原子结构示意图为。
(2)硫酸铝溶液与过量氨水反应的离子方程式为。
(3)能证明
溶液中存在
 水解平衡的事实是(填序号)。
水解平衡的事实是(填序号)。
A.滴人酚酞溶液变红,再加人
溶液后红色退去
B.滴人酚酞溶液变红,再加人氯水后红色退去
C.滴人酚酞溶液变红,再加人
溶液后产生沉淀且红色退去
(4)元素
、
在周期表中位于向一主族,化合物
和
可发生如下转化(其中
是纤维素水解的最终产物):
① 非金属性
(填">"或"<")
②
与过量浓硝酸反应有红棕色气体生成,化学方程式为
(5)在恒容绝热(不与外界交换能量)条件下
 反应,按下表数据投料,反应达到平衡状态,测得体系压强升高。简述该反应的平衡常数与温度的变化关系:
反应,按下表数据投料,反应达到平衡状态,测得体系压强升高。简述该反应的平衡常数与温度的变化关系:
| 物质 |
||||
| 起始投料/ | 2 |
1 |
2 |
0 |
直接排放煤燃烧产生的烟气会引起严重的环境问题,将烟气通过装有石灰石浆液的脱硫装置可以除去其中的二氧化硫,最终生成硫酸钙。硫酸钙可在下图所示的循环燃烧装置的燃料反应器中与甲烷反应,气体产物分离出水后得到几乎不含杂质的二氧化碳,从而有利于二氧化碳的回收利用,达到减少碳排放的目的。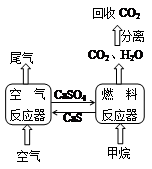
请回答下列问题:
(1)煤燃烧产生的烟气直接排放到空气中,引发的主要环境问题有。(填写字母编号)
| A. | 温室效应 | B. | 酸雨 | C. | 粉尘污染 | D. | 水体富营养化 |
(2)在烟气脱硫的过程中,所用的石灰石浆液在进入脱硫装置前,需通一段时间二氧化碳以增加其脱硫效率;脱硫时控制浆液的
值,此时浆液含有的亚硫酸氢钙可以被氧气快速氧化生成硫酸钙。
①二氧化碳与石灰石浆液反应得到的产物为。
②亚硫酸氢钙被足量氧气氧化生成硫酸钙的化学方程式为。
(3)已知1mol
在燃料反应器中完全反应生成气态水时吸收160.1
,1
在氧气中完全燃烧生成气态水时放热802.3
。写出空气反应器中发生的热化学方程式:。
(4)回收的
与苯酚钠在一定条件反应生成有机物M,其化学式为
,
经稀硫酸酸化后得到一种药物中间体
,N的结构简式为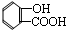 。
。
①M的结构简式为。
②分子中无
,醛基与苯环直接相连的N的同分异构体共有种。
下列框图中的字母分别代表一种常见的物质或其溶液,相互之间的转化关系如图所示(部分产物及反应条件已略去)。已知
为气态单质,
是地壳中含量最多的金属元素的单质,
为氧化物,
为黑色固体,
为红棕色气体,
为红褐色沉淀。
请回答下列问题:
(1)
中所含元素位于周期表中第周期族。
(2)
在
中燃烧的现象是。
(3)
的反应中,被氧化与被还原的物质的量之比是。
(4)
的离子方程式是。
(5)
受热分解的化学方程式是。
PET是世界上产量最大的合成纤维,其结构简式为
原料,设计合成PET的工业生产流程如下(反应中部分无机反应物及产物未表示):
请回答下列问题:
(1)发生反应①需加入的反应物及其条件是_____________、_____________;
发生反应②的反应物及反应条件是_____________、_____________。
(2)过程⑤的反应类型是_____________。
(3)写出反应③的化学方程式_______________________________________。
(4)有机物A有多种同分异构体,写出满足下列条件的A的一种同分异构体X的结构简式:____。
①在X中滴入FeCl3溶液呈紫色,②X分子结构中只有一个甲基,③1molX分别与足量的金属钠、NaOH溶液反应,消耗n(Na):n(NaOH)=2:1。
(5)从D到E,工业上一般通过二步反应来完成。有人从原子利用率100%的角度提出通过D与某种无机物质一步合成E,该无机物是_____________。
在有机合成中,Diels—Alder反应可用于合成环状有机物。
例如:
若用键线式表示,则上述反应可写成: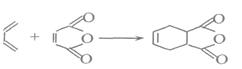
已知:①两个双键同时连在一个碳原子上不是稳定结构。
②CH2=CH—CH=CH2+X2 X—CH2一CH=CH—CH2一X(X2=F2、C12、Br2)。
X—CH2一CH=CH—CH2一X(X2=F2、C12、Br2)。
现以某直链烃A为起始原料合成化合物J。合成路线如下图所示(图中Mr表示相对分子质量)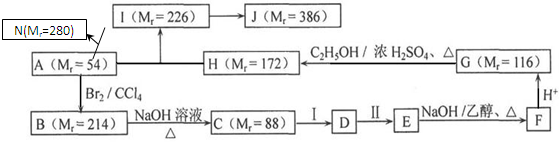
根据题给信息和所学知识同答下列问题:
(1)C中的官能团为。
(2)G的结构简式为。
(3)指出B C的反应类型。
C的反应类型。
(4)写出下列反应的化学方程式:
①G H:。
H:。
②A+I N:。
N:。
(5)根据E的结构判断,它可能发生的化学反应有(填字母)。
| A.取代反应 | B.加成反应 | C.加聚反应 | D.消去反应 E.中和反应 |
(6)反应I、II中有一步反应是与HCl加成,该反应是(填:I或II);设计这一步反应的目的是。