“宏观辨识与微观探析”是化学学科核心素养之一,化学学习要让学生既能够“见微知著”,也能够“见著知微”。
金属钠在氯气中燃烧生成氯化钠,如图为氯化钠形成的示意图。
根据所给信息,请回答:
(1)钠原子的核外电子层数是 ,在化学反应中易 (填“得到”或“失去”)电子。
(2)元素的化学性质主要是由原子的 决定的。
(3)化学反应前后,氯元素的化合价变化为 。
(4)构成氯化钠的离子是 (填微粒符号)。

化学改变世界,科技改变生活。
请回答:

(1)我国自主研发的复兴号动车组列车,领跑世界,其制造材料有铝合金等,在空气中铝制品耐腐蚀的原因是 。
(2)我国对石墨烯技术的研究居世界领先地位。石墨烯性能优良,用途独特,比如用作太阳能电池的电极,这主要是利用了它的 性。
(3)我国自主设计建造的港珠澳大桥是目前世界最长的跨海大桥,它使用了世界最大尺寸高阻尼橡胶隔震支座,其中橡胶属于 (填字母)。
a.金属材料 b.有机高分子材料 c.复合材料
(4)我国在氢能汽车研发领域取得重大突破,采用了第四代以氢为燃料的电池技术。
氢气作为理想能源前景广阔,氢气燃烧的化学方程式为 ,氢能源的优点是 (答出一点即可)。
我国煤炭资源丰富。某实验室设计的利用水煤浆(由煤和水混合而成)制备氢气的生产工艺如图流程一所示。
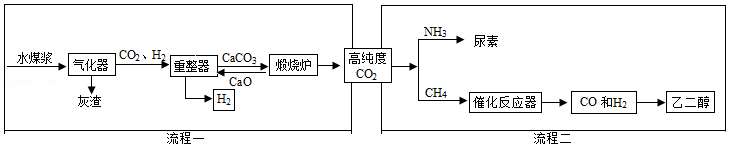
[流程一]制备氢气。
(1)气化器中发生的主要反应为:Ⅰ.H2O+C CO+H2;Ⅱ.CO+H2O CO2+H2,其中属于置换反应的是 (填“Ⅰ”或“Ⅱ”),反应Ⅱ中发生还原反应的物质是 。
(2)重整器的作用是 。重整器中发生反应的化学方程式是 。
(3)该流程中可以循环使用的物质是 。
[流程二]为充分利用流程一产生的高纯度二氧化碳,该实验室又设计了如图中流程二所示的两种工艺分别制备尿素和乙二醇。
(1)在高温高压下,CO2和NH3可以合成尿素[CO(NH2)2],同时生成水,该反应的化学方程式为 。尿素属于化肥中的 肥,能使作物枝叶繁茂。
(2)以CO和H2为原料生产乙二醇(C2H6O2)时,按照“绿色化学”原则,应调节原料中CO和H2的分子个数比为 。
烟台有漫长的海岸线,蕴藏着丰富的海洋资源。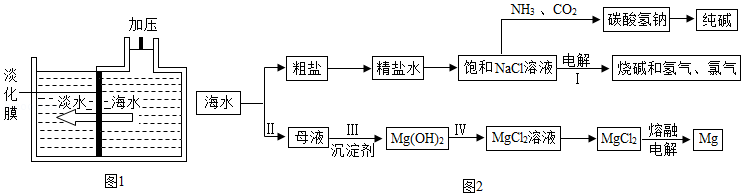
(1)海水淡化。可以采用如图1所示的膜分离法淡化海水,水分子可以通过淡化膜(海水中体积较大的盐的离子和其他分子不能通过)进入左侧的淡水池,从而得到淡水。下列说法中正确的是 (填字母序号)。
A.膜分离法的原理与滤纸过滤原理类似
B.膜分离法还可以浓缩海水中的盐类物质
C.膜分离法也是一种分离混合物的方法
D.该膜分离法的目的是除去海水中的不溶物
(2)粗盐提纯。除去难溶性杂质后的食盐水中还含有Ca2+、Mg2+、SO42﹣等杂质离子,为得到较纯的氯化钠,进行如下的实验操怍①加入过量的Na2CO3溶液;②加入过量的BaCl2溶液③加入过量的NaOH溶液; ④加入适量的盐酸调节溶液的pH等于7;⑤过滤;⑥蒸发。下列操作顺序正确的是 (填字母序号),其中操作④加入适量的盐酸调节溶液的pH等于7的目的是 。
A.①③②④⑤⑥
B.③②①④⑤⑥
C.③①②⑤④⑥
D.②③①⑤④⑥
(3)海水资源综合利用的部分途径如图2。
①氨碱工业生产过程中,在加压并不断向饱和的氨盐水中通入二氧化碳的条件下,使碳酸氢钠结晶析出,该反应的化学方程式是 。
②写出步骤Ⅰ电解饱和NaCl溶液的化学方程式是 。
③海水制镁。实际生产中,步骤Ⅲ常选用 作为沉淀剂,从海水中提取MgCl2历经步骤Ⅱ、Ⅲ、Ⅳ三步转换的主要目的是 。
2018年12月8日,搭载着“嫦娥四号”探测器的“长征三号乙”运载火箭发射成功。
(1)“长征三号乙”火箭发动机在焊接时需要使用氩弧焊。氩弧焊(如图)是在氩气保护下,通过在钨电极与焊件间产生的高压电弧放热,熔化焊丝或焊件的一种焊接技术。
①金属钨作电极是利用了金属钨的导电性和 ;用氩气作保护气,是因为氩气的化学性质 。
②如果在没有保护气的情况下焊接金属,可能导致焊接不牢,原因是 。
(2)“长征三号乙”的第一、二子级火箭用偏二甲肼(C2H8N2)和四氧化二氮(N2O4)做推进剂,该反应的化学方程式为C2H8N2+2N2O4=3N2+4H2O+2X,则X的化学式是 。
(3)“长征三号乙”的第三子级火箭采用液氢、液氧做推进剂。实验室可采用电解水得到氢气和氧气,氢气在与直流电源 极相连的电极上产生。氢能是未来最理想的能源,但目前应用并不广泛的原因是 (答一条即可)。
(4)“嫦娥四号”光伏发电板的主要构成材料是硅,单质硅由石英固体(SiO2)和碳在高温下反应制得,同时产生一种可燃性气体,该反应的化学方程式是 。
