某短周期元素原子最外层电子数为次外层的2倍,其单质甲可发生:
甲+乙 丙+丁+水。
丙+丁+水。
(1)若丙为NO2。①甲与乙反应的化学方程式为 。
② NO2可作火箭重要燃料—肼(N2H4)的助燃剂。N2(g)+2O2(g)=2NO2(g) △H=+67.7kJ·mol-1,2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g) △H=—1135.7 kJ·mol-1,写出肼(N2H4)燃烧生成氮气和水蒸气的热化学方程式: 。
(2)若丙为SO2。①把乙滴入硫酸铜晶体,观察到的现象是 。
②完成SO2使KMnO4褪色的离子方程式: MnO4- + SO2 + = Mn2+
+ SO42- + H+
③一定条件下:2SO2(g)+O2(g)  2SO3(g) △H<0。反应的平衡常数表达式K= ;反应达平衡时,若改变其中一个条件x,则符合图中曲线的是
2SO3(g) △H<0。反应的平衡常数表达式K= ;反应达平衡时,若改变其中一个条件x,则符合图中曲线的是 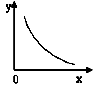
a.x表示温度,y表示n(SO2) b.x表示压强,y表示SO2的转化率
c.x表示n(SO2),y表示n(O2) d.x表示n(SO3),y表示化学平衡常数K
【化学——选修5:有机化学基础】
已知某有机物A为烃类化合物,其相对分子质量为70,各物质之间的转化关系如下图所示,其中B、D、E的结构中均含有2个甲基,且核磁共振氢谱都有4个峰。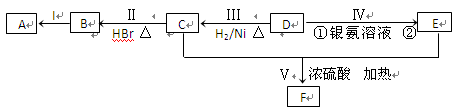
(1)A的分子式为,D中所含官能团的名称为。
(2)I的反应条件为,Ⅲ的反应类型为。
(3)写出反应Ⅳ中①的化学方程式。
(4)写出反应Ⅴ的化学方程式。
(5)E有多种同分异构体。其中:
①能发生银镜反应,又能与金属钠反应生成氢气,但不能发生消去反应:;
②能在酸性条件下水解,且两种水解产物相对分子质量相同:。
【化学——选修3:物质结构与性质】
用黄铜矿(主要成分是CuFeS2)生产粗铜的反应原理如下: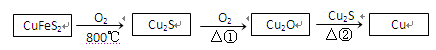
(1)已知在反应①、②中均生成相同的气体分子,该气体具有漂白性。请分别写出反应①、
②的化学方程式是、。
(2)基态铜原子的核外电子排布式为,硫、氧元素相比,第一电离能较大的是。
(3)反应①和②生成的气体分子的中心原子的杂化类型是,分子的空间构型是。
(4)某学生用硫酸铜溶液与氨水做了一组实验,CuSO4溶液中加氨水生成蓝色沉淀,再加氨水沉淀溶解,得到深蓝色透明溶液,最后向该溶液中加入一定量乙醇,析出[Cu(NH3)4]SO4·H2O晶体,请解释加入乙醇后析出晶体的原因;在该晶体中存在化学键的种类有。
(5)Cu2O的晶胞结构如图所示,该晶胞的边长为a cm,则Cu2O的密
度为g·cm-3(用NA表示阿伏加德罗常数的数值)。
【化学——选修2:化学与技术】
以黄铁矿(主要成分是FeS2)为原料生产硫酸的工艺流程图如下:
(1)沸腾炉中发生反应的化学方程式为;接触室中发生反应的化学方程式是。
(2)沸腾炉出来的炉气需要精制,如果不经过精制,对SO2催化氧化的影响是
(3)硫酸工业是一种易造成多种形式污染的工业,工业上常采用氨—酸法进行尾气脱硫,以达到消除污染、废物利用的目的。用化学方程式表示其反应原理:;对矿渣的合理利用方法是。
(4)某工厂用500t 含硫量为48%的黄铁矿制备硫酸,若在沸腾炉中有2%的FeS2损失,在接触室中SO3的产率为96%,则可得到98%的浓硫酸的质量是t。
短周期元素形成的常见非金属固体单质A与常见金属单质B,在加热条件下反应生成化合物C,C与水反应生成白色沉淀D和无色、有臭鸡蛋气味的气体E,D既能溶于强酸,也能溶于强碱。E分子含18个电子,在足量空气中燃烧生成G,G在大气中能导致酸雨的形成。E被足量氢氧化钠溶液吸收得到无色溶液F。溶液F在空气中长期放置发生反应,生成物之一为H。H与过氧化钠的结构和化学性质相似,其溶液显黄色。
(1)组成单质A的元素位于周期表中第周期第族;
(2)化合物H的电子式为;
(3)B与氢氧化钠溶液反应的离子方程式为:;
(4)G与氯酸钠溶液反应可生成消毒杀菌剂二氧化氯。写出对应的离子方程式:
(5)溶液F在空气中长期放置生成H的化学反应方程式为:;
(6)写出F溶液中各离子浓度由大到小的关系为:;
工业生产纯碱的工艺流程示意图如下: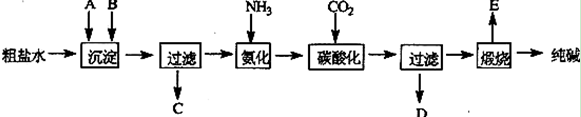
完成下列填空:
(1)粗盐水加入沉淀剂A、B除杂质(沉淀剂A来源于石灰窑厂),实验室提纯粗盐的实验操作依次为:取样、溶解、沉淀、 、蒸发、冷却结晶、 、烘干。
(2)工业生产纯碱工艺流程中,碳酸化时产生的现象是 。
碳酸化时没有析出碳酸钠晶体,其原因是 。
(3)碳酸化后过滤,滤液D最主要的成分是 (填写化学式),检验这一成分的阴离子的具体方法是: 。
(4)氨碱法流程中氨是循环使用的,为此,滤液D加入石灰乳产生氨。加石灰水后所发生的反应的离子方程式为: 。
(5)产品纯碱中含有碳酸氢钠。取a克产品用加热分解的方法测定纯碱中碳酸氢钠的质量分数,充分加热并在干燥器中冷却得b克固体。纯碱中碳酸氢钠的质量分数可表示为:。