反应4A(g) + 5B(g) 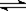 4C(g) + 6D(g) △H =-Q kJ/mol,在一定温度下达到化学平衡状态时,下列说法正确的是:
4C(g) + 6D(g) △H =-Q kJ/mol,在一定温度下达到化学平衡状态时,下列说法正确的是:
A.若增大压强,A和B的转化率都增大
B.若升高温度最终能生成更多的C和D
C.单位时间里有4n mol A消耗,同时有5n mol B生成
D.容器里A、B、C、D的浓度比是4:5:4:6
两种一元碱MOH和ROH的溶液分别加水稀释,溶液pH的变化如图所示,下列叙述不正确的是
| A.MOH是一种弱碱 |
| B.在x点,c(M+)=c(R+) |
| C.稀释前,c(ROH)=10 c(MOH) |
| D.稀释前MOH溶液和ROH溶液中由水电离出的c(OH-)前者是后者的 10倍 |
根据表中信息,判断下列叙述中正确的是
| 序号 |
氧化剂 |
还原剂 |
其他反应物 |
氧化产物 |
还原产物 |
| ① |
Cl2 |
FeBr2 |
/ |
Cl- |
|
| ② |
KClO3 |
浓盐酸 |
/ |
Cl2 |
|
| ③ |
KMnO4 |
H2O2 |
H2SO4 |
O2 |
Mn2+ |
A.表中①组的反应可能有一种或两种元素被氧化
B.氧化性强弱的比较: KClO3>Fe3+>Cl2>Br2
C.表中②组反应的还原产物是KCl,电子转移数目是6e-
D.表中③组反应的离子方程式为:2MnO4-+ 3H2O2 + 6H+=2Mn2+ + 4O2↑+ 6H2O
将pH=3的盐酸a L分别与下列三种溶液混合,混合后溶液均呈中性,其中a、b、c、d的关系正确的是
①1×10-3 mol·L-1的氨水b L
②c(OH-)=1×10-3 mol·L-1的氨水c L
③c(OH-)=1×10-3 mol·L-1的Ba(OH)2溶液d L
| A.b>a=d>c | B.a=b>c>d |
| C.a=b>d>c | D.c>a=d>b |
下列化学用语书写正确的是
A.NaHS水解反应:HS-+ H2O H3O++ S2- H3O++ S2- |
| B.明矾加入在水中起净化作用的原因: Al3++ 3H2O=Al(OH)3(胶体) + 3H+ |
| C.已知: 2Zn(s)+O2(g)=2ZnO(s);△H=-701.0kJ·mol-1 2Hg(l)+O2(g)=2HgO(s);△H=-181.6kJ·mol-1 则反应Zn(s)+ HgO(s)=ZnO(s)+ Hg(l);△H=-259.7kJ·mol-1 |
| D.碳酸氢钠溶液中加入过量Ba(OH)2溶液: |
2HCO3- + Ba2+ + 2OH- = BaCO3↓+ CO32-+ 2H2O
化学工业在经济发展中的作用举足轻重,下列有关工业生产的叙述中正确的是
| A.氯碱工业中阳极得到氢氧化钠和氢气 |
| B.电镀铜时,电镀液中c(Cu2+)基本保持不变 |
| C.合成氨中采取及时分离液态氨来提高反应速率 |
| D.海水中含有钾元素,只需经过物理变化就可以得到钾单质 |