.(16分)某课外活动小组同学用下图装置进行实验,试回答下列问题。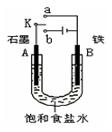
(1)若开始时开关K与a连接,则B极的电极反应式为 。
(2)若开始时开关K与b连接,则B极的电极反应式为 ,总反应的离子方程式为 ,有关该实验的下列说法正确的是(填序号) 。
①溶液中Na+向A极移动 ②从A极处逸出的气体能使湿润KI淀粉试纸变蓝 ③反应一段时间后加适量盐酸可恢复到电解前电解质的浓度 ④若标准状况下B极产生2.24 L气体,则溶液中转移0.2 mol电子
(3)该小组同学模拟工业上用离子交换膜法制烧碱的方法,设想用下图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。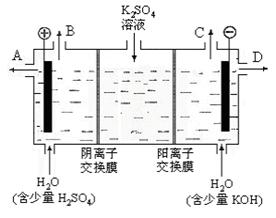
①该电解槽的阳极反应式为 。此时通过阴离子交换膜的离子数 (填“大于”或“小于”或“等于”)通过阳离子交换膜的离子数。
②制得的氢氧化钾溶液从 出口 (填写“A”、“B”、“C”、“D”)导出。
③通电开始后,阴极附近溶液pH会增大,请简述原因 。
④若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池,则电池正极的电极反应式为 。
Ⅰ、 (1)某化学兴趣小组欲从下列装置中选取必要的装置制取 (NH4)2SO4溶液,连接的顺序(用接口序号字母表示)是:a
(2)将装置C中两种液体分离开的操作名称是_________。
装置D的作用是。
Ⅱ、为提高氯化铵的经济价值,我国化学家设计了利用氢氧化镁热分解氯化铵制氨气并得到碱式氯化镁(MgOHCl)的工艺。某同学根据该原理设计的实验装置如图:
请回答下列问题:
(1) 装置A中发生反应生成碱式氯化镁的化学方程式为_________ ____
装置B中碱石灰的作用是_______
(2) 反应过程中持续通入N2的作用有两点:一是使反应产生的氨气完全导出并被稀硫酸充分吸收,二是_____________________
(3) 装置C的试管中反应的离子方程式为______________
乙酸乙酯是常见酯类化合物,其实验室制备提纯过程如下:
制备反应:CH3COOH+CH3CH2OH  CH3COOC2H5+H20
CH3COOC2H5+H20
实验步骤:
①按照下图制备装置组装一起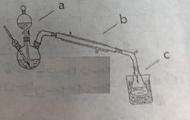
②在三颈瓶中加入4mL乙醇,慢慢振荡加入5mL浓硫酸。仪器a内装预先混合均匀的10mL乙醇和8mL乙酸
③先从a中放出3mL混合液,于石棉网上加热110-120℃.有馏分分出时,打开a活塞,控制流速(每分钟30滴)。至滴加完毕无馏分时停止加热。
④摇动盛粗产品的锥形瓶,向其中加入饱和碳酸钠溶液至有机相呈中性。
⑤将液体转入分液漏斗中,摇振后静置,弃水相。有机相依次用饱和食盐水洗涤后和饱和氯化钙溶液洗涤,每次均弃水相。
⑥有机相转入干燥的锥形瓶,加无水硫酸镁干燥。
试回答:
1、仪器a、b的名称分别为______ 、______。
2、实验步骤②加入过量的乙醇的目的是。还需要加入______。
3、实验步骤5中摇荡静置后如图所示,请写出弃水相的操作。
4、试写出实验过程中发生的副反应的方程式:乙醇被浓硫酸脱水碳化同时放出SO2:。
5、步骤③中滴加速度过快会使乙酸乙酯的产率降低,造成产率降低的原因可能是:
①
②
某实验小组利用如下装置(部分固定装置略)制备氮化钙(Ca3N2),并探究其实验式。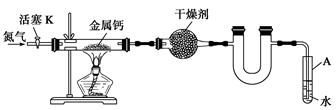
(1)反应过程中末端导管必须始终插入试管A的水中,目的是_____________________。
(2)制备氮化钙的操作步骤是:
①打开活塞K并通入N2;
②点燃酒精灯,进行反应;
③反应结束后,__________________________________________________________;
④拆除装置,取出产物。
(3)数据记录如下:(假设反应完全)
| 空硬质管质 量m0/g |
硬质管与钙的 质量m1/g |
硬质管与产物 的质量m2/g |
| 14.80 |
15.08 |
15.15 |
① 计算得到实验式CaxN2,其中x=________。
②若通入的N2中混有少量O2,请比较x与3的大小,并给出判断依据:
______________________________________________________________________。
明矾石是制取钾肥和氢氧化铝的重要原料,明矾石的组成和明矾相似,此外还含有氧化铝和少量的氧化铁杂质。具体实验流程如下: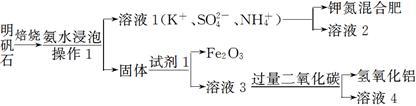
请回答下列问题:
(1)操作1所用到的玻璃仪器的名称是____________。
(2)由溶液3制取氢氧化铝的离子方程式为。
(3)请你写出验证溶液1中有NH4+的实验过程:_______________________________________________。
(4)实验室用Fe2O3与CO反应来制取单质Fe。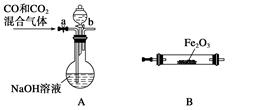
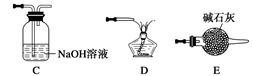
①请按气流由左到右的方向连接下列各装置,顺序为A→。
②检查装置A气密性的方法是。
③在点燃B处的酒精灯前,应进行的操作是_______________________________________;④装置C的作用是________________。
50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题: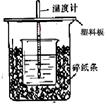
(1)从实验装置上看,图中尚缺少的一种玻璃用品_____ ___。
(2)烧杯间填满碎纸条的作用是___________________________。
(3)大烧杯上如不盖硬纸板,求得的中和热数值(填“偏大”、“偏小”、“无“影响”)。
(4)实验中60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量(填“相等”、“不相等”),所求中和热(填“相等”、“不相等”),简述理由。