某同学按如图所示装置进行实验,A、B为常见金属,它们的硫酸盐可溶于水。当K闭合时,在交换膜处SO42-从右向左移动,系列分析正确的是() 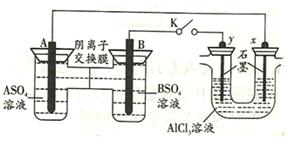
A.溶液中(A2+)浓度减小
B.B的电极反应为:B-2e-=B2-
C.y电极上有氢气产生,发生还原反应
D.反应初期x电极周围出现白色胶状沉淀,不久沉淀溶解
下列关于催化剂的说法正确的是
| A.使用催化剂可以增大正反应速率,减小逆反应速率 |
| B.使用催化剂可以使化学平衡向正反应方向移动 |
| C.使用催化剂可以降低反应的活化能 |
| D.使用催化剂可以改变反应的平衡常数 |
一种有机物燃烧后产生CO2、H2O、SO2,则该化合物中可能不含有的元素是
| A.C | B.H | C.O | D.S |
下列有关碱金属铷(Rb)的叙述中,正确的是()
| A.铷与水反应的现象与钠相似 | B.硝酸铷易溶于水 |
| C.在钠、钾、铷三种单质中,铷的熔点最低 | D.氢氧化铷是弱碱 |
下列关于元素周期表的说法正确的是
| A.周期表里主族元素所在的族序数等于原子核外电子数 |
| B.周期表里元素所在的周期序数等于原子核外电子层数 |
| C.元素周期表有7个主族,7个副族,1个0族,1个第Ⅷ族,共16纵行 |
| D.X2+的核外电子数目为18,则X在第四周期第ⅡA族 |
日本核泄漏事故释放的放射性物质中含有碘-131,下列关于131 53I的说法正确的是
| A.131 53I和134 53I是同一种核素 | B.131 53I 和134 53I互为同位素 |
| C.131 53I 和134 53I都含有53个电子 | D.131 53I 和134 53I都含有53个中子 |