铜在常温下能被稀HNO3溶解:3Cu+8HNO3(稀)="=" 3Cu(NO3)2+2NO↑+4H2O
⑴ 请将上述反应改写成离子方程式:_____________________。
⑵ 上述反应中氧化剂是 ,没有参加氧化还原反应的硝酸占总硝酸的比例_____。
(3)取1.92gCu与一定量浓HNO3恰好完全反应,生成气体颜色由红棕色逐渐变成无色,共得到标准状况下气体1.12L,则参加反应的硝酸为_____________mol。
(1)铀主要以三种同位素的形式存在,三种同位素的原子百分含量分别为: U 0.005%、
U 0.005%、 U 0.72%、
U 0.72%、 U 99.275%。请列出计算U元素近似原子量的计算式(不必算出具体数值):___________。
U 99.275%。请列出计算U元素近似原子量的计算式(不必算出具体数值):___________。
(2)放射性同位素40Co能够产生γ射线。高速运动的γ射线作用于DNA,能够产生氢键断裂、碱基替换等效应,从而有可能诱发生物产生___________,使生物体出现可遗传的变异,从而选择和培育出优良品种。此外用γ射线照射过的食品有利于贮藏,这是因为γ射线能___________。在进行照射生物或食品的操作时,需要注意人体防护。操作完毕后,人体___________ (可以、不可以)直接触摸射线处理过的材料。
Zn+2MnO2+2NH ===Zn2++Mn2O3+2NH3+H2O
===Zn2++Mn2O3+2NH3+H2O
(1)试写出干电池放电时的正、负电极反应式:正极:___________负极:___________
干电池用久了就会变软,其原因是____________________________________________。
(2)正极反应中,前后经历了下列两个反应:
2NH +2e-===2NH3+H2
+2e-===2NH3+H2
2MnO2+H2===Mn2O3+H2O
如果正极反应没有MnO2的参与,干电池将难以持续稳定工作。试说明理由。
(3)在通电10 min的时间内参加反应的MnO2质量约为多少?外电阻消耗的电能是多少?
(4)许多国家对废旧电池进行回收,从保护环境和节约能源解释为什么要回收废旧电池。
阳极反应式:2CO+2CO
 4CO2+4e-
4CO2+4e-
阴极反应式:,总电池反应式:。
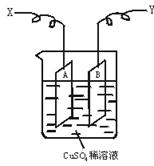
(1)当以I="0.21" A的电流电解60 min后,测得铜片A的质量增加了0.25 g,则图装置中的X端应与直流电的__________极相连,它是电解池的__________极。
(2)电解后铜片B的质量__________。(答“增加”“减少”或“不变”)
(3)列式计算实验测得的阿伏加德罗常数NA。(已知电子电量e=1.60×10-19C)
CO2+4H2 ()+2H2O
()+2H2O
若将CO2与H2混合,在一定条件下以1∶3的比例发生反应,生成某种重要的化工原料和水。该化工原料可能是
| A.烷烃 | B.烯烃 | C.炔烃 | D.芳香烃 |