利用碱性氧化性溶液的氧化作用,在钢铁表面形成一层Fe3O4薄膜,保护内部金属免受腐蚀,这种方法叫做烤蓝。烤蓝时发生如下反应:
①3Fe+NaNO2+5NaOH===3Na2FeO2+H2O+NH3↑
②Na2FeO2+NaNO2+H2O===Na2Fe2O4+NH3↑+NaOH(未配平)
③Na2FeO2+Na2Fe2O4+2H2O===Fe3O4+4NaOH
下列说法中不正确的是
| A.Fe3O4既可看做是氧化物,又可看做是亚铁盐 |
| B.反应②配平后,H2O的化学计量数为3 |
| C.反应③是非氧化还原反应 |
| D.碱性条件下,NaNO2的氧化性比Na2FeO2、Na2Fe2O4都强 |
已知BrCl能发生下列反应(M为+n价的金属元素):
nBrCl + 2M ="==" MCl n + MBr n BrCl + H2O ="==" HCl + HBrO
以下结论不正确的是:
| A.BrCl具有和卤素单质相似的化学性质 |
| B.BrCl与M反应时,BrCl只作氧化剂 |
| C.BrCl与NaOH溶液反应生成NaCl和NaBrO两种盐 |
| D.BrCl与H2O的反应中,BrCl既作氧化剂又作还原剂 |
将下列选项中的两种气体X和Y同时通入盛有足量氯化钡溶液的洗气瓶中(如右图装置),肯定无沉淀产生的是()
| A.碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y |
| B.碳跟浓硫酸共热产生的气体X和铜跟稀硝酸反应产生的气体Y |
| C.MnO2跟浓盐酸共热产生的气体X和碳跟浓硫酸共热产生的气体Y |
| D.碳跟浓硫酸共热产生的气体X和NH4Cl与Ca(OH)2共热产生的气体Y |
下列各组中的离子,能够大量共存于同一溶液中的是
| A.NO3—、 Fe2+、 Na+、H+ | B.H+ 、Ag+、Cl— 、SO42— |
| C.OH—、CO32-、Na+、NO3— | D.HCO3—、Na+、OH—、Mg2+ |
下列反应的离子方程式正确的是
| A.Cl2通入水中: Cl2+H2O=2H++Cl-+ClO- |
B.往碳酸镁中滴加稀盐酸: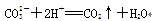 |
| C.硫酸铜溶液和氢氧化钡溶液:Ba2++SO42—=BaSO4↓ |
| D.稀硝酸与铜反应:8H+ + 2NO3—+ 3Cu="==3" Cu2++2NO↑+4H2O |
下列说法中,正确的是
| A.除去液溴中少量的氯水,可向其中加少量KI |
| B.氯水和氯气均能使湿润的有色布条褪色,都是HClO作用的结果 |
| C.能与硝酸银反应生成白色沉淀的溶液中一定含有Cl— |
| D.某溶液能使淀粉碘化钾试纸变蓝,则溶液中一定含有Cl2 |