(1)某温度下纯水中c(H+) = 2×10-7 mol/L,则此时水中的C(OH-) =mol/L,若温度不变,向水中滴入稀盐酸使C(H+) = 5×10-6 mol/L,则此时溶液中的c(OH-) = __ mol/L,滴入盐酸后水的离子积(填“变大”“变小”或“不变”,下同),水的电离度。
(2)今有A、 CH3COOH; B、 HCl;C、 H2SO4三种溶液,
①当它们pH相同时,其物质的量浓度关系是(用字母表示, 下同);
下同);
②体积和物质的量浓度相同的三种溶液,分别与同浓度的烧碱溶液反应,要使反应后的溶液呈中性,所需烧碱溶液的体积关系为;
③当它们pH相同、体积相同时,分别加入足量锌,相同状况下产生气体体积关系为。
高炉炼铁过程中发生的主要反应为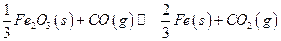
已知该反应在不同温度下的平衡常数如下:
请回答下列问题:
(1)该反应的平衡常数表达式K =_____________,△H______0(填“>”、“<”或“=”);
=_____________,△H______0(填“>”、“<”或“=”);
(2)在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0 mol,反应经过l0 min后达到平衡。求该时间范围内反应的平均反应速率
υ(CO2)= _____________、CO的平衡转化率= ___________;
(3)欲提高(2)中CO的平衡转化率,可采取的措施是__________。
| A.减少Fe的量 | B.增加Fe2O3的量  |
C.移出部分CO2 |
| D.提高反应温度 E.减小容器的容积 F.加入合适的催化剂 |
烟气中NOx是NO和NO2的混合物(不含N2O4)。 (1)根据废气排放标准,1m3烟气最高允许含400 mg NOx。若NOx中NO质量分数为0.85,则1m3烟气中最高允许含NO__________L(标准状况,保留2位小数)。
(1)根据废气排放标准,1m3烟气最高允许含400 mg NOx。若NOx中NO质量分数为0.85,则1m3烟气中最高允许含NO__________L(标准状况,保留2位小数)。 (2)工业上通常用溶质质量分数为0.150的Na2CO3水溶液(密度1.16g/mL)作为NOx吸收剂,该碳酸钠溶液物质的量浓度为____________mol/L(保留2位小数)。
(2)工业上通常用溶质质量分数为0.150的Na2CO3水溶液(密度1.16g/mL)作为NOx吸收剂,该碳酸钠溶液物质的量浓度为____________mol/L(保留2位小数)。 (3)已知:
(3)已知: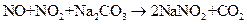 ①
①
 ②
②
1m3 含2000 mg NOx的烟气用质量分数为0.150的碳酸钠溶液吸收。若吸收率为80%,吸收后的烟气_______排放标准(填“符合”或“不符合”),理由:______________。
含2000 mg NOx的烟气用质量分数为0.150的碳酸钠溶液吸收。若吸收率为80%,吸收后的烟气_______排放标准(填“符合”或“不符合”),理由:______________。 (4)加入硝酸可改变烟气中NO和NO2的比,反应为:
(4)加入硝酸可改变烟气中NO和NO2的比,反应为: NO+2HNO3→3NO2+H2O
NO+2HNO3→3NO2+H2O 当烟气中
当烟气中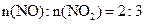 时,吸收率最高。
时,吸收率最高。
1m3烟气含2000 mg NOx,其中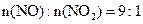 。
。 计算:①为了达到最高吸收率,1m3烟气需用硝酸的物质的量(保留3位小数)。
计算:①为了达到最高吸收率,1m3烟气需用硝酸的物质的量(保留3位小数)。 ②1m3烟气达到最高吸收率90%时,吸收后生成NaNO2的质量(假设上述吸收反应中,反应①比反应②迅速。计算结果保留1位小数)。
②1m3烟气达到最高吸收率90%时,吸收后生成NaNO2的质量(假设上述吸收反应中,反应①比反应②迅速。计算结果保留1位小数)。
2SO2(g)+O2(g) =2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3的ΔH=-99kJ·mol-1.请回答下列问题: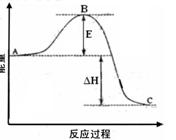
 (1)图中A.C分别表示.,E的大小对该反应的反应热有无影响?。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?,理由是;
(1)图中A.C分别表示.,E的大小对该反应的反应热有无影响?。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?,理由是; (2)图中△H=KJ·mol-1;
(2)图中△H=KJ·mol-1; (3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式;
(3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式; (4)已知单质硫的燃烧热为296 KJ·mol-1,计算由S(s)生成3 molSO3(g)的△H
(4)已知单质硫的燃烧热为296 KJ·mol-1,计算由S(s)生成3 molSO3(g)的△H
(写出计算过程)
有4种化合物W(通常状况下是气态).X(通常状况下是液态).Y、Z(通常状况下是固态),它们共由5种短周期元素A、B、C、D、E组成。已知:①原子序数A<B<C<D<E,且A与D同族;C与E同族;B与C同周期。②W由A和B组成,且W分子中,A与B的原子个数比为4∶1;X由A和C组成,且X分子中A与C的原子个数比为1∶1,Y由C和D组成,属离子化合物,且测得Y固体中C与D的原子个数比为1∶1。③Z由D和E组成,属离子化合物,且其阳离子比阴离子少1个电子层,阳离子数与阴离子数之比为2∶1。试推断写出:
(1)W的化学式是,W属于分子(填极性或非极性)。
(2)X的电子式是,X属于化合物。
(3)1 mol Y在干燥的空气中质量会(填“增大”或“减小”),其变化量(Δm)为。
(4)用电子式表示化合物Z的形成过程。