(10分)按分子结构决定性质的观点可推断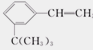 有如下性质:
有如下性质:
(1)苯环部分可发生______反应和__________反应;
(2)—CH=CH2部分可发生_______反应和_______反应;
(3)该有机物滴入溴水后生成产物的结构简式为_____。
某一溴代烷A与氢氧化钠溶液混合后充分振荡,生成有机物B;A在氢氧化钠和B的混合液中共热生成一种气体C;C可由B与浓H2SO4混合加热制得,C可作果实催熟剂。则:
(1)A的结构简式为:______________________。
(2)A生成B的化学方程式:______________________。
(3)A生成C的化学方程式:______________________。
(4)B生成C的反应类型:______________________。
在NaCl溶液中滴入AgNO3溶液,现象为_____________________,离子方程式为_____________________。在CH3CH2Cl中滴加AgNO3溶液,现象为______________________,原因是______________________。若将CH3CH2Cl跟NaOH溶液共热,然后用稀HNO3酸化,再滴入AgNO3溶液,现象为______________,反应的化学方程式为______________________。
下列物质中:
 ⑤NaHSO3溶液
⑤NaHSO3溶液
(1)能与NaOH溶液发生反应的是____________。
(2)能与溴水发生反应的是___________。
(3)能与金属钠发生反应的是___________。
A、B、C、D四种芳香族化合物的结构简式如下所示: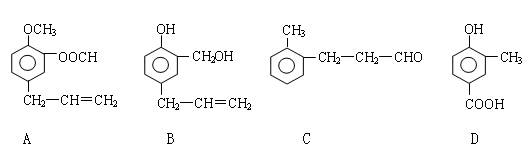
请回答下列问题:
(1)写出A中无氧官能团的名称 ;D中含氧官能团的结构简式为 。
(2)用A、B、C、D填空:能发生银镜反应的有 ;既能与FeCl3溶液发生显色反应又能与Na2CO3溶液反应放出气体的是 。
(3)按下图C经一步反应可生成E,E是B的同分异构体,
则反应①的反应类型为 ;写出反应②的化学方程式: 。
(4)G、H和D互为同分异构体,它们具有如下特点:
① G和H都是苯的二元取代物,这两个取代基分别为羟基和含有-COO-结构的基团;
② G和H苯环上的一氯代物有两种不同结构;
③ G可以发生银镜反应,H分子中苯环不与取代基碳原子直接相连 。
写出G和H的结构简式:G: ;H: 。
A~I分别表示中学化学中常见的一种物质,它们之间相互关系如下图所示(部分反应物、生成物没有列出),且已知G为主族元素的固态氧化物,A、B、C、D、E、F六种物质中均含同一种元素。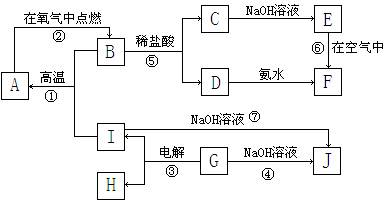
请填写下列空白:
(1)I、G、J三种物质中所含同一种元素在周期表中位置第_______周期、第_______族;
(2)写出反应⑥的化学方程式____________________;
(3)写出反应④的离子方程式____________________;
(4)若28g A单质在足量的氧气中灼烧,反应放出的热量为Q kJ(Q > 0),写出这个反应的热化学方程式:;
(5) 反应⑦中若有18g I参与反应,则转移电子数为NA。