下列说法或表示方法中正确的是( )
| A.吸热反应中,新化学键形成吸收能量;放热反应中,新化学键形成放出能量 |
| B.等质量的硫蒸气和硫磺分别完全燃烧,后者放出的热量多 |
| C.相同体积浓度均为0.1 mol/L 盐酸和醋酸溶液分别与足量的NaOH稀溶液反应,前者放出热量多 |
| D.氢气的燃烧热为285.8 kJ/mol,则氢气燃烧的热化学方程式为:2H2(g)+O2(g)===2H2O(l) ΔH=-285.8 kJ/mol |
完全燃烧一定质量的无水乙醇,放出的热量为Q,为完全吸收生成的CO2,并使之生成正盐Na2CO3,消耗掉0.8mol/L NaOH溶液500mL,则燃烧1mol酒精放出的热量是
| A.0.2Q | B.0.1Q | C.5Q | D.10Q |
下列反应达到平衡后,增大压强或升高温度,平衡都向正反应方向移动的是
A.2NO2(g)  N2O4(g)△H<0 N2O4(g)△H<0 |
B.3O2(g) 2O3(g)△H>0 2O3(g)△H>0 |
C.H2(g)+I2(g) 2 H I(g)△H<0 2 H I(g)△H<0 |
D.NH4HCO3(s) NH3(g)+H2O(g)+CO2(g)△H>0 NH3(g)+H2O(g)+CO2(g)△H>0 |
如图所示曲线表示其它条件一定时反应2NO(g)+O2(g) 2NO2(g)△H<0,NO的转化率与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达平衡状态且V(正)>V(逆)的点是
2NO2(g)△H<0,NO的转化率与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达平衡状态且V(正)>V(逆)的点是
| A.a点 | B.b点 | C.c 点 | D.d点 |
将H2(g)和Br2(g)充入恒容密闭容器,恒温下发生反应H2(g)+Br2(g) 2 HBr(g)△H<0,平衡时Br2转化率为a;若初始条件相同,绝热下进行上述反应,平衡时Br2转化率为b,则a、b的关系是
2 HBr(g)△H<0,平衡时Br2转化率为a;若初始条件相同,绝热下进行上述反应,平衡时Br2转化率为b,则a、b的关系是
| A.a>b | B.a=b | C.a<b | D.无法确定 |
今有X(g)+Y(g) 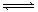 2Z(g) △H<0。从反应开始经过t1后达到平衡状态,t2时由于条件改变,平衡受到破坏,在t3时又达到平衡,引起t2→t3曲线变化的原因是
2Z(g) △H<0。从反应开始经过t1后达到平衡状态,t2时由于条件改变,平衡受到破坏,在t3时又达到平衡,引起t2→t3曲线变化的原因是
| A.增大X或Y的浓度 | B.增大压强 |
| C.增大Z的浓度 | D.升高温度 |