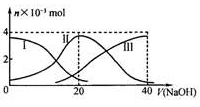
常温下,向20 mL 0.2 mol/L H2A溶液中滴加0.2 mol/L NaOH溶液。有关微粒的物质的量变化如下图(其中I代表H2A,II代表HA-,III代表A2-)。根据图示判断,下列说法正确的是
A.当V(NaOH)="20" mL时,溶液中离子浓度大小关系:c(Na+)>c(HA¯)>c(H+)> c(A2-)>c(OH¯)
B.等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中 水的电离程度比纯水的大
C.NaHA溶液中:c(OH—)+c(A2–)=c(H+)+c(H2A)
D.向Na2A溶液加入水的过程中,pH可能增大也可能减小
一种新型的高温结构陶瓷主要成分为含碳和氮两种元素的化合物,则该化合物的化学式可能为()
| A.CN | B.C2N3 | C.C3N4 | D.C4N3 |
锗酸铋简称(BGO)是我国研制成功的一种闪烁晶体材料,其中锗(Ge)元素处于最高价态,铋元素(Bi)的价态与铋跟氯形成某种共价氯化物时所呈的价态相同,且在氯化物中铋具有最外层8电子的稳定结构。GBO的化学式是()
| A.Bi3Ge3O15 | B.Bi4Ge3O12 | C.Bi4Ge3O16 | D.Bi3Ge3O12 |
下列说法不正确的是()
| A.新型无机非金属材料具有光学特性、生物功能、电学特性、耐高温、强度高 |
| B.高温结构陶瓷比金属材料具有许多优点,如不怕氧化、密度小等优点 |
| C.氮化硅陶瓷属于新型无机非金属材料,但不是高温结构材料 |
| D.光导纤维除用于通讯外,还可以用于医疗、信息处理等许多方面 |
2001年报道硼和镁形成的化合物刷新了金属化合物最高温度的记录。右示意图是该化合物的晶体结构单元:镁原子间形成正六棱柱,且棱柱的上下底面还各有1个镁原子;6个硼原子位于棱柱内(未画出)。则该化合物的化学式可表示为()
| A.MgB | B.MgB2 | C.Mg2B | D.Mg3B2 |
下列除去杂质的方法正确的是( )
| A.用加热法除去Na2CO3固体中的NaHCO3 |
| B.用加热法除去MnO2固体中的KMnO4 |
| C.用加热法除去SiO2中的Na2SiO3 |
| D.用加热法除去SiO2中的CaCO3 |