根据如下2005年十大科技进展的报道,回答问题:
材料1:法国科学家利用特种显微仪器,让一个分子做出了各种动作。这一成果使人类能精确控制单个分子运动,进而开发出分子机器人。
材料2:中科院上海硅酸盐研究所研制出了“药物分子运输车”。这种分子装载药物后,被引导到疾病靶点释放药物,对疾病进行高效治疗。
(1)材料1和2研究的粒子是________;构成物质的粒子还有________________;
(2)分析上述材料,谈谈你对“分子总是在不断运动着”的新认识:___________________;
(3)在阿西莫夫所写的科幻小说《梦幻航行》中,人被缩小到细胞般大小,在人体内经历了梦幻般的体验。试想,如果你被缩小到一个原子般大小,把你放到水里,你会看到的景象是(请至少写两点):
化学与健康--从化学的视角看食品添加剂。
从化学的视角看食品添加剂,主要是从其元素组成与结构、物理化学性能及在人体内的变化等方面来研究。结合表中信息回答下列问题。
| 物质的组成与性能 |
用于食品添加剂 |
|||
| 物质名称 |
物质组成 |
主要化学性质及在体内变化 |
类别或作用 |
法律规定 |
| 碳酸氢钠 |
NaHCO3 |
无毒、弱碱性,易与胃酸反应,加热分解成碳酸钠、水和二氧化碳 |
膨松剂 |
可用 |
| 铁 (还原性铁粉) |
Fe |
比较活泼的金属,能与胃酸反应 |
抗氧化剂 |
依据国家标准可用 |
| 食盐 |
NaCl |
易溶、中性,与硝酸银溶液反应生成白色沉淀 |
调味剂 |
可用 |
| 甲醛 |
CH2O |
 |
防腐 |
国家严禁使用 |
| 亚硝酸钠 |
NaNO2 |
易溶、水溶液显碱性,跟硝酸银反应生成浅黄色沉淀 |
发色剂、防腐剂 |
严格依据国家标准 |
(1)国家严格禁止甲醛作为食品添加剂的原因是。
(2)还原性铁粉用于食品添加剂,除能够防止食品因氧化而变质外,还是一种营养强化剂,这是因为。
(3)碳酸氢钠是面食类食品经常使用的添加剂,如蒸馒头时人们常常加适量的碳酸氢钠,其作用是,写出发生反应的化学方程式。
(4)亚硝酸钠(
)外观酷似食盐,有咸味,常被误作食盐食用而导致中毒事件发生。有一包外观酷似食盐的固体,结合表中信息,如何鉴别它是亚硝酸钠还是氯化钠(包括选取的试剂、方法、实验现象和结论,只写出一种方法即可)。
(5)从改善食品的色香味、延长食品的保质期等方面,食品添加剂确实提高了现代食品的品质,但副作用也是显而易见的。我们需要食品添加剂吗?你的观点是。
“孔雀石”的主要成分是碱式碳酸铜[Cu2(OH)2CO3],它是一种重要的铜矿石原料。小明欲从孔雀石中提炼出单质铜。
【查阅资料】(1) 碱式碳酸铜加热易分解,其方程式为:Cu2(OH)2CO3加热2CuO+CO2↑+H20。
(2) 向Cu2(OH)2CO3中加入足量的盐酸,固体完全溶解,有无色气体生成,写出此反应的化学方程式: 。
【设计方案】在实验室中以碱式碳酸铜、铁粉、稀盐酸为原料来制取单质铜。请你仿照下图画出方案二制取铜的流程图,要求:步骤最少。
方案一: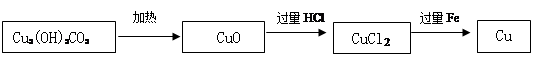
方案二:你设计的方案为
【进行实验】方案一中最后一步:在溶液中加入过量的Fe的实验现象为
【反思】铜锈的主要成分也是碱式碳酸铜,从碱式碳酸铜的化学式[Cu2(OH)2CO3]推知,铜生锈可能与空气中的氧气、水、________________________有关。
(9分)我国制碱工业的先驱侯德榜将制碱与制氨结合起来的联合制碱法,为纯碱和氮肥工业技术的发展做出了杰出的贡献。其生产工艺流程示意图如下:
【资料】四种盐在不同温度下的溶解度表
| 10℃ |
20℃ |
30℃ |
40℃ |
50℃ |
|
| NaCl |
35.8 |
36.0 |
36.3 |
36.6 |
37.0 |
| NH4HCO3 |
15.8 |
21.0 |
27.0 |
—— |
—— |
| NaHCO3 |
8.1 |
9.6 |
11.1 |
12.7 |
—— |
| NH4Cl |
33.3 |
37.2 |
41.4 |
45.8 |
50.4 |
⑴检验粗盐水是否为硬水的方法是加入;
⑵操作a是,生产流程中被循环利用的物质是;
⑶在精盐水中先通入NH3,使溶液呈性,再通入CO2,有利于对CO2的吸收;
⑷氨盐水中通入二氧化碳后,在常温条件下,易析出NaHCO3晶体而不析出NH4Cl晶体的可能原因是;
⑸粗盐水中主要含有CaCl2、MgCl2等杂质,工业上常加入下列物质除杂、精制,则加入下列三种试剂合理的顺序为(填序号);
A.适量的盐酸 B.稍过量的Na2CO3溶液 C.稍过量的Ca(OH)2溶液
⑹副产品NH4Cl可做肥,若加入氢氧化钠加热,反应的化学方程式为。
.海水是巨大的资源宝库。下图是综合利用海水制备的一些产品的流程: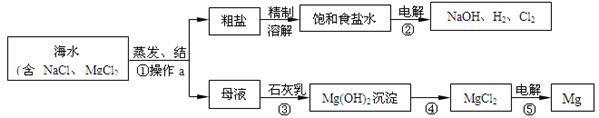
(1)操作a 的名称是,在实验室中完成此项操作需要的玻璃仪器有烧杯、玻璃棒和。
(2)步骤①中用蒸发结晶法而不采用降温结晶法的理由是。
(3)步骤④应加入的物质是。
(4)请写出步骤②、③发生反应的化学方程式:
②,③。
一辆有约30吨硝酸的罐车在某厂道路发生侧翻,硝酸泄露,散发出黄色烟雾,流到石灰石地面,发出嘶嘶声,产生大量气泡,泄露出来的硝酸不断流进路边的排水沟,气味十分刺鼻.
(1)由题给信息可知,硝酸的物理性质是 _________ (任写一条)
(2)硝酸见光后,除分解生成二氧化氮气体外,还生成水及占空气体积分数约21%的气体,实验室保存硝酸应密封,遮光保存在棕色瓶内,放在低温阴凉处,硝酸见光分解的化学方程式为 _________
(3)为消除硝酸对环境的污染,对泄露的酸必须处理,经济上合理、对环境污染小的化学处理方法是 ________ .