(6分)对于下列反应:2SO2 + O2  2SO3,如果2min内SO2的浓度由6 mol/L下降为2 mol/L,那么,用SO2 浓度变化来表示的化学反应速率为___ ________,用O2浓度变化来表示的反应速率为_________ ____。如果开始时SO2浓度为4mol/L,2min后反应达平衡,若这段时间内v(O2)为0.5mol/(L·min),那么2min时SO2的浓度为__ 。
2SO3,如果2min内SO2的浓度由6 mol/L下降为2 mol/L,那么,用SO2 浓度变化来表示的化学反应速率为___ ________,用O2浓度变化来表示的反应速率为_________ ____。如果开始时SO2浓度为4mol/L,2min后反应达平衡,若这段时间内v(O2)为0.5mol/(L·min),那么2min时SO2的浓度为__ 。
按要求完成下列填空
Ⅰ.已知:①2C3H8(g)+7O2(g)=6CO(g)+8H2O(l) ΔH=-2741.8kJ/mol
②2CO(g)+O2(g)=2CO2(g)ΔH="-566" kJ/mol
(1)反应C3H8(g)+5O2(g)=3CO2(g)+4H2O(l)的ΔH=;
(2)C3H8在不足量的氧气里燃烧,生成CO和CO2以及气态水,将所有的产物通入一个固定体积的密闭容器中,在一定条件下发生如下可逆反应:CO(g)+ H2O(g) 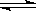 CO2(g)+ H2(g) ΔH>0
CO2(g)+ H2(g) ΔH>0
①下列事实能说明该反应达到平衡的是;
a.体系中的压强不发生变化
b.υ正(H2)=υ逆(CO)
c.混合气体的平均相对分子质量不发生变化
d.CO2的浓度不再发生变化
②在某温度下,反应物的起始浓度分别为:c(CO)=" 1" mol·L-1, c(H2O)="2.4" mol·L-1; 达到平衡后,CO的转化率为60%,该反应在此温度下的平衡常数是;
(3)熔融碳酸盐燃料电池的电解质为Li2CO3和 Na2CO3的混合物,燃料为CO,在工作过程中,电解质熔融液的组成、浓度都不变,写出负极发生的电极反应式。
Ⅱ.氮化硅(Si3N4)是一种新型陶瓷材料,它可用石英与焦炭在高温的氮气流中反应制得:
SiO2+C +N2 Si3N4+CO根据题意完成下列各题:
Si3N4+CO根据题意完成下列各题:
(1)配平上述化学反应方程式。SiO2+C +N2 Si3N4+CO
Si3N4+CO
(2)为了保证石英和焦炭尽可能的转化,氮气要适当过量。某次反应用了30mol氮气,反应生成了5mol一氧化碳,则此时混合气体的平均摩尔质量是。
(3)氮化硅陶瓷的机械强度高,硬度接近于刚玉(A12O3),热稳定性好,化学性质稳定。以下用途正确的是。
| A.可以在冶金工业上制成坩埚、铝电解槽衬里等设备 |
| B.在电子工业上制成耐高温的电的良导体 |
| C.研发氮化硅的全陶发动机替代同类型金属发动机 |
| D.氮化硅陶瓷的开发受到资源的限制,没有发展前途 |
(14分)绿矾(FeSO4·7H2O)是治疗缺铁性贫血药品的重要成分。下面是以市售铁屑(含少量锡、氧化铁等杂质)为原料生产纯净绿矾的一种方法: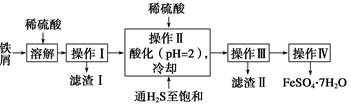
查询资料,得有关物质的数据如下表:
| 25 ℃时 |
pH值 |
| 饱和H2S溶液 |
3.9 |
| SnS沉淀完全 |
1.6 |
| FeS开始沉淀 |
3.0 |
| FeS沉淀完全 |
5.5 |
(1)操作Ⅱ中,通入硫化氢至饱和的目的是____________;在溶液中用硫酸酸化至pH=2的目的是_______________________________________________________。
(2)操作Ⅳ的顺序依次为蒸发浓缩、冷却结晶、___________________________。
(3)操作Ⅳ得到的绿矾晶体用少量冰水洗涤,其目的是:①除去晶体表面附着的硫酸等杂质②_____________。
(4)测定绿矾产品中Fe2+含量的方法是:a.称取2.850 g绿矾产品,溶解,在250 mL容量瓶中定容;b.量取25.00 mL待测溶液于锥形瓶中;c.用硫酸酸化的0.010 00 mol·L-1 KMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00 mL。
①滴定时盛放KMnO4溶液的仪器为________(填仪器名称)。
②判断此滴定实验达到终点的方法是_____________________________________。
③计算上述样品中FeSO4·7H2O的质量分数为_______________________________。
(12分)Ⅰ.某反应中反应物与生成物有: AsH3、H2SO4、KBrO3、K2SO4、H3AsO4、H2O和一种未知物单质X。
(1)写出反应的化学方程式:__________________________________________________。
(2)根据上述反应可推知________。
a.氧化性:KBrO3>H3AsO4
b.氧化性:H3AsO4>KBrO3
c.还原性:AsH3>X
d.还原性:X>AsH3
Ⅱ.常见的五种盐A、B、C、D、E,它们的阳离子可能是Na+、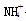 、Cu2+、Ba2+、Al3+、Ag+、Fe3+,阴离子可能是Cl-、NO3-、SO42-、CO32-,已知:
、Cu2+、Ba2+、Al3+、Ag+、Fe3+,阴离子可能是Cl-、NO3-、SO42-、CO32-,已知:
①五种盐均溶于水,水溶液均为无色。
②D的焰色反应呈黄色。
③A的溶液呈中性,B、C、E的溶液呈酸性,D的溶液呈碱性。
④若在这五种盐的溶液中分别加入Ba(NO3)2溶液,只有A、C的溶液不产生沉淀。
⑤若在这五种盐的溶液中,分别加入氨水,E和C的溶液中生成沉淀,继续加氨水,C中沉淀消失。
⑥把A的溶液分别加入到B、C、E的溶液中,均能生成不溶于稀硝酸的沉淀。请回答:
(3)所含阴离子相同的两种盐的化学式是________________________________。
(4)A的化学式为________,D溶液显碱性的原因是(用离子方程式表示): ______________________。
(5)若要检验B中所含的阳离子,正确的实验方法是_________________________________________。
(14分)CH4和CO2反应可以制造价值更高的化学产品。
(1)250℃时,以镍合金为催化剂,向4 L容器中通入6 mol CO2、6 mol CH4,发生反应:CO2 (g)+CH4(g) 2CO(g)+2H2(g)。达到平衡时CH4的物质的量为2mol。
2CO(g)+2H2(g)。达到平衡时CH4的物质的量为2mol。
①此温度下,该反应的平衡常数K=________(注明单位)。
②保持温度不变,改变CH4和CO2的初始物质的量之比,充入容器进行反应,下列描述能够说明体系处于平衡状态的是(填序号)。
a.容器内气体平均相对分子质量不随时间改变
b.混合气体的密度不随时间改变
c.单位时间内生成a mol CO2的同时消耗2a mol H2
d.混合气中n(CH4)∶n(CO2)∶n(CO)∶n(H2) =1∶1∶4∶4
③已知:a.CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H1kJ·mol-1
b.CO(g)+H2O (g)=CO2(g)+H2 (g) △H2kJ·mol-1
c.2CO(g)+O2(g)=2CO2(g) △H3kJ·mol-1
反应CO2(g)+CH4(g) 2CO(g)+2H2(g)的△H="__" kJ·mol-1
2CO(g)+2H2(g)的△H="__" kJ·mol-1
(2)用Cu2Al2O4做催化剂,一定条件下,发生反应:
CO2+CH4 CH3COOH,温度与催化剂的催化效率和乙酸的生成速率如图。
CH3COOH,温度与催化剂的催化效率和乙酸的生成速率如图。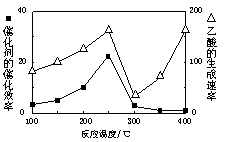
250~300℃时,温度升高而乙酸的生成速率降低的原因是_________________________ __________。
(3)Li2O、Na2O、MgO均能吸收CO2,
①若寻找吸收CO2的其他物质,下列建议合理的是_________。
A.可在碱性氧化物中寻找
B. 可在具有强氧化性的物质中寻找
C.在ⅠA、ⅡA族元素的氧化物中寻找
②Li4SiO4可用于吸收、释放CO2, 原理是: 500℃时,CO2与Li4SiO4接触生成Li2CO3;平衡后加热至700℃,反应逆向进行,放出CO2,Li4SiO4再生,该原理的化学方程式___________ ____________________________________。
(4)以NO2、O2、熔融NaNO3组成的燃料电池装置如图所示,在使用过程中石墨Ⅰ电极反应生成一种氧化物Y,有关电极反应可表示为______________________。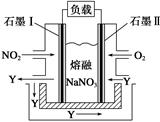
(15分)由香兰素制取多巴胺的,合成过程如下: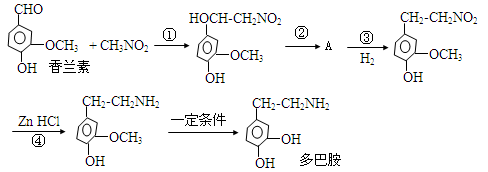
请回答下列问题:
(1)香兰素除了醛基之外,还含有官能团的名称是。
(2)多巴胺的分子式是。
(3)上述合成过程中属于加成反应类型的是:(填反应序号)。
(4)写出符合下列条件的多巴胺的其中一种同分异构体的结构简式:
①属于1,3,5-三取代苯;②苯环上直接连有一个羟基和一个氨基;③分别能与钠和氢氧化钠反应,消耗钠与氢氧化钠的物质的量之比为2∶1。_________________________
(5)请写出有机物A与足量浓溴水反应的化学方程式。
___________________________________________________________________________