如图是电解CuCl2溶液的装置,其中c、d为石墨电极。则下列有关的判断正确的是( )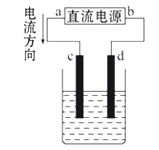
| A.a为负极,b为正极 |
| B.a为阳极,b为阴极 |
| C.电解过程中,d电极质量增加 |
| D.电解过程中,氯离子浓度不变 |
五彩缤纷的焰火与元素的焰色反应有关。下列说法错误的是
| A.观察K2SO4的焰色应透过蓝色的钴玻璃 |
| B.Na与NaCl在灼烧时火焰颜色相同 |
| C.可以用焰色反应来区别NaCl和KCl |
| D.焰色反应一定发生化学变化 |
光导纤维已成为信息社会必不可少的高技术材料。下列物质用于制造光导纤维的是
| A.金刚石 | B.大理石 | C.铝合金 | D.二氧化硅 |
脂肪酸平衡是保证营养平衡的条件之一,食用油提供了人所需要的大部分脂肪酸,因此注意食用油的摄入是保持人体中脂肪酸均衡的重要因素。在日常生活中选购食用油时,最便捷的保证脂肪酸平衡的方法是
| A.更换不同的食用油 | B.将不同的油混合后食用 |
| C.食用按一定比例配比的调和油 | D.食用喜欢吃的油 |
蛋白质是人体必需的重要营养成分之一。下列食物中,富含蛋白质的是
| A.豆腐 | B.馒头 | C.西红柿 | D.油脂 |
苹果汁是人们喜爱的饮料,由于此饮料中含有Fe2+,鲜榨苹果汁在空气中会由浅绿色变为棕黄色。若榨汁时加入维生素C,可有效防止这种现象发生。这说明维生素C具有
| A.氧化性 | B.还原性 | C.碱性 | D.酸性 |