将氯化铝溶液蒸干灼烧并熔融后用铂电极进行电解,下列有关电极产物的判断正确的是
| A.阴极产物是氢气 | B.阳极产物是氧气 |
| C.阴极产物是铝和氧气 | D.阳极产物是氯气 |
有反应2A(g)+B(g)  2C(g)△H =Q,下列叙述正确的是[ ]
2C(g)△H =Q,下列叙述正确的是[ ]
| A.增大压强,v正增大,v逆减小 |
| B.升高温度,v正减小,v逆增大 |
| C.增大A浓度的瞬间,v正增大,v逆不变 |
| D.增大A浓度瞬间,v正增大而v逆减小 |
已知热化学方程式:2H2(g)+O2(g)=2H2O(g) ΔH1=-483.6kJ/mol,则对于热化学方程式:2H2O(l)=2H2(g)+O2(g) ΔH2=b,下列说法正确的是[ ]
| A.该反应的ΔH2=+483.6kJ/mol | B.|ΔH2|<|ΔH1| |
| C.|ΔH2|>|ΔH1| | D.热化学方程式中化学计量数表示分子个数 |
下列热化学方程式中的反应热为可燃物的燃烧热的是[ ]
| A.H2(g)+1/2O2(g)=H2O(g) △H =-241.8kJ·mol—1 |
| B.CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H =-846.3kJ·mol—1 |
| C.C(s)+O2(g)=CO2(g) △H =-393.5kJ·mol—1 |
| D.C3H8(g)+5O2(g)=3CO(g)+4H2O(l)△ H = -2044.0kJ·mol—1 |
人造象牙主要成分的结构是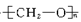 ,它是通过加聚反应制得的,则合成象牙的单体是[ ]
,它是通过加聚反应制得的,则合成象牙的单体是[ ]
| A.HCHO | B.CH3CHO |
| C.CH3OCH3 | D.C2H2和H2O |
在a g冰醋酸、甲醛、葡萄糖、甲酸甲酯、果糖的混合物中,碳元素的质量分数为[ ]
| A.30% | B.40% |
| C.50% | D.数据不全,无法计算 |