工业炼铁是在高炉中进行的,高炉炼铁的主要反应是:① 2C(焦炭)+O2(空气)=2CO;② Fe2O3+3CO=2Fe+3CO2该炼铁工艺中,对焦炭的实际使用量要远高于按照化学方程式计算所需,可能的主要原因是:
| A.炼铁高炉的高度不够 | B.CO与铁矿石接触不充分 |
| C.CO过量 | D.CO与Fe2O3的反应有一定限度 |
| A.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,说明有Ca2+ |
| B.通入Cl2后,溶液变为黄色,加入淀粉溶液后溶液变蓝,说明有I- |
| C.往溶液中加入盐酸,产生的气体能使澄清石灰水变浑浊,说明有CO32— |
| D.往溶液中加入 BaC12溶液和稀 HNO3 ,有白色沉淀生成,说明有SO42- |
合成氨工业对国民经济和社会发展具有重要的意义。哈伯法合成氨需要在20~50MPa的高压和500℃左右的高温下,并用铁触媒作为催化剂,氨在平衡混合物中的含量仍较少。最近英国俄勒冈大学的化学家使用了一种名为 trans一Fe(DMeOPrPE)2的新催化剂,在常温下合成氨,反应方程式可表示为N2 +3H2 2NH3 .有关说法正确的是
2NH3 .有关说法正确的是
| A.哈伯法合成氨是吸热反应,新法合成氨是放热反应 |
| B.新法合成氨不需要在高温条件下,可节约大量能源,具有发展前景 |
| C.新法合成氨能在常温下进行是因为不需要断裂化学键 |
| D.新催化剂降低了反应所需要的能量,提高了活化分子百分数 |
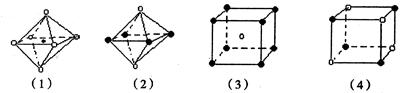
| A.图(1)和图(3) | B.图(2)和图(3) | C.图(1)和图(4) | D.只有图(4) |
| A.焊接时用 NH4C1 溶液除锈 |
| B.使用泡沫灭火器时,使硫酸铝与饱和小苏打溶液混合 |
| C.饱和氯化铁溶液滴入沸水制备 Fe(OH)3胶体 |
| D.生活中用电解食盐水的方法制取消毒液 |
| A.1mol 任何气体单质在标况下体积都约为22.4L,含有的原子数都为2×6.02×1023 |
| B.同温、同压、同体积的氢气和氧气具有相同的分子数 |
| C.在铁与硫的反应中,1mol 铁失去的电子数为3×6.02×1023 |
| D.在pH="13" 的 NaOH 溶液中,OH-的数目为0.1×6.02×1023 |