水的电离过程为H2O  OH-+H+ ,在25℃、35℃时其离子积分别为K(25℃)=1×10-14 、K(35℃)=2.1×10-14 。则下列叙述中正确的是( )
OH-+H+ ,在25℃、35℃时其离子积分别为K(25℃)=1×10-14 、K(35℃)=2.1×10-14 。则下列叙述中正确的是( )
| A.在35℃,纯水中C(H+)>C(OH-) |
| B.水的电离度α(25℃)>α(35℃) |
| C.25℃时,向纯水中加入盐酸或氢氧化钠都能使水的电离平衡逆向移动,水的离子积减小 |
| D.某温度下纯水中C(H+) 为2×10-7 mol/L,则此时的C(OH-) 也为2×10-7 mol/L |
化学与生活生产、环境保护、资源利用、能源开发等密切相关。下列说法不正确的是()
| A.实施“雨污分流”工程,可提高水资源的利用率 |
| B.煤的气化、液化是使煤变成清洁能源的有效途径 |
| C.绿色化学的核心是应用化学原理对环境污染进行治理 |
| D.合理开发利用可燃冰(固态甲烷水合物)有助于缓解能源紧缺 |
下图所示装置中,a、b、c、d、e、f均为惰性电极,电解质溶液均足量。接通电源后,d极附近显红色。下列说法正确的是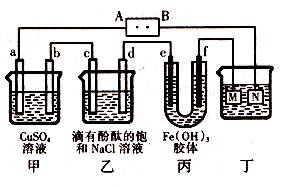
| A.电源B端是正极 |
| B.a、c电极均有单质生成,其物质的量之比为2:1 |
| C.欲用丁装置给铜镀银,N应为Ag,电解液为AgNO3溶液 |
| D.f极附近变红,说明氢氧化铁胶粒带正电荷 |
下图为元素周期表短周期的一部分。E原子的电子层数为n,最外层电子数为2n+1下列叙述不正确的是
A.C和E氢化物的热稳定性和还原性均依次减弱
B.A与B形成的阴离子可能有AB32- A2B42-
C.AD2分子中每个原子的最外层均为8电子结构
D.A、D、E的最高价氧化物对应的水化物的酸性依次增强
下列图示与对应的叙述相符的是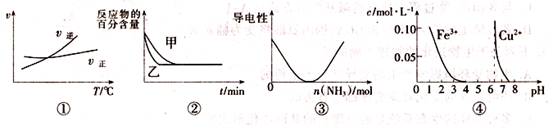
A.据图①可判断可逆反应A2(g)+3B2(g) 2AB3(g)的ΔH>0 2AB3(g)的ΔH>0 |
B.图②表示压强对可逆反应2A(g)+B(g) 3C(g)+D(g)的影响,乙的压强大 3C(g)+D(g)的影响,乙的压强大 |
| C.图③可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化 |
| D.据图④,若除去0.1mol·L-1CuSO4溶液中混有的Fe3+,可向溶液中加入适量NaOH至pH约为7 |
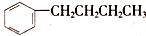 的同分异构体中,某苯环上的一氯代物只有一种的结构有(不考虑立体异构)
的同分异构体中,某苯环上的一氯代物只有一种的结构有(不考虑立体异构)
| A.6种 | B.5种 | C.4种 | D.3种 |