现有四种元素的基态原子的电子排布式如下:① 1s22s22p63s23p4;②1s22s22p63s23p3;③1s22s22p5。则下列有关比较中正确的是
| A.第一电离能:③>②>① | B.原子半径:③>②>① |
| C.电负性:③>②>① | D.最高正化合价:③>②>① |
化学在生产和生活中有着广泛的应用。下列说法错误的是
| A.用聚乙烯塑料作食品包装袋 |
| B.SiO2是制备光纤导线的主要材料 |
| C.用铝锅炒菜比用铁锅好 |
| D.用明矾作净水剂除去水中的悬浮物 |
已知X、Y、Z为三种由短周期元素构成的10个电子的粒子,其结构特点如下:
| 粒子代码 |
X |
Y |
Z |
| 原子核数 |
单核 |
两核 |
四核 |
| 粒子的电荷数 |
一个单位正电荷 |
一个单位负电荷 |
0 |
物质A由X、Y构成, B、C、D、K都是单质,各有关物质之间的相互反应转化关系如下图所示,反应①~⑤都是用于工业生产的反应,反应⑥中个别产物在图中略去。请填写下列空白: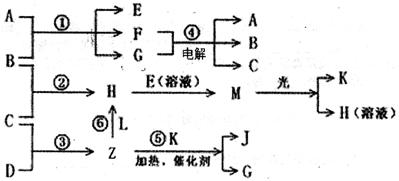
(1)Y的化学式是_______,Z分子的空间构型为_______,A的电子式为_______。
(2)写出下列反应的离子反应方程式:
H+E(溶液)→M________________________________________________________
F+G→A+B+C_____________________________________________
(3)L是由3种元素构成的分子,能与Z以1:2的物质的量之比反应生成尿素CO(NH2)2和物质H,写出L的结构式:____________。
(4)常温下,实验室模拟工业反应④的过程如右图所示,标况下,当电极上产生112mL(已折算为标准状况下的体积)B气体时,烧杯中溶液的pH=______。(假设气体完全逸出,溶液体积不变)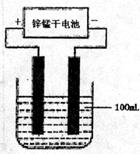
相同温度下,体积均为0.5 L的两个恒容密闭容器中发生可逆反应:
2XY2(g)+Y2(g) 2XY3(g),
2XY3(g),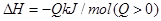
实验测得反应在起始、达到平衡时的有关数据如下表所示:
| 容器 |
起始时各物质物质的量/mol |
达平衡时体系能量的变化 |
||
| 编号 |
XY2 |
Y2 |
XY3 |
|
| ① |
2 |
1 |
0 |
放热0.25QkJ |
| ② |
1.2 |
0.6 |
0.8 |
下列叙述不正确的是
A.达到平衡时,①和②两容器中气体的平均相对分子质量相同
B.容器②中反应达到平衡时放出的热量为0.15 Q kJ
C.达到平衡时,两个容器中Y2的物质的量浓度均为1.5 mol·L-1
D.若容器①的其他条件不变,只增加1mol稀有气体,则达到平衡时放出的热量等于0.25 Q kJ
全钒液流电池是一种新型的绿色环保储能电池。其电池总反应为: 。下列说法正确的是
。下列说法正确的是
A.放电时正极反应为: |
B.充电时阴极反应为: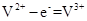 |
| C.放电过程中电子由负极经外电路移向正极,再由正极经电解质溶液移向负极 |
| D.充电过程中,H+由阴极区向阳极区迁移 |
中草药秦皮中含有的七叶树内酯( ),它具有抗菌作用。关于七叶树内酯的说法正确的是
),它具有抗菌作用。关于七叶树内酯的说法正确的是
| A.七叶树内酯的官能团只有l种 |
| B.1mol七叶树内酯与足量的溴水和氢氧化钠完全反应消耗3 mol Br2和4 mol NaOH |
| C.七叶树内酯中所有的原子一定都在同一平面 ‘ |
| D.七叶树内酯的分子式为C9H5O4 |