.(12分)有V、W、X、Y、Z五种元素,它们的核电荷数依次增大,且都小于20;只有X、Z是金属元素;V和Z元素原子的最外层电子都只有一个;W和Y 元 素原子的最外层电子数相同,且W元素原子L层电子数是K层电子数的3倍;X元素原子的最外层电子数是Y元素原子最外层电子数的一半。由此可知:
(1)Y元素最高价氧化物对应水化物的分子式为 ,Z元素最高价氧化物对应水化物的化学键类型 ______________。
(2)V与W形成的常见三原子分子化合物的电子式为 。
(3)Y与Z形成的化合物属于 (填“离子化合物”或“共价化合物”)。
(4)写出X分别与盐酸和NaOH溶液反应的离子方程式:___________________________,______________________________
已知M2+离子3d轨道上有5个电子,则
(1)M原子的外围电子排布图(轨道表示式)为:。
(2)M原子的最外层电子数为个;最高能级中电子数为个。
(3)M元素在周期表中的位置是:。
已知A 是一种分子量为28的气态烃,现以A为主要原料合成一种具有果香味的物质E,其合成路线如下图所示。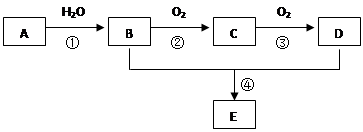
请回答下列问题:
(1)写出A的结构简式 。
(2)B、D分子中的官能团名称分别是 , 。
(3)物质B可以被直接氧化为D,需要加入的试剂是。
(4)写出下列反应的化学方程式:
①;反应类型:。
④;反应类型:。
现有短周期的三种元素X、Y、Z,原子序数依次变小,原子核外电子层数之和为5。X元素原子最外层上的电子数是Y元素原子最外层与Z元素原子最外层电子数之和;Y元素最外层上电子数是其电子层数的2倍,X和Z可以形成XZ3型化合物,请回答问题:
(1) X的名称_________,Y的名称_________,Z的名称_________。
(2) XZ3的化学式为________,电子式为______,分子间存在________键。
(3)X最高价氧化物对应水化物的浓溶液与红热的Y单质反应的化学方程式为____________________________。
在2升容器中加入18g水蒸气,28g一氧化碳,在t℃时(t>100),发生如下反应:
CO+H2O CO2+H2,在最初5秒钟内,一氧化碳的平均反应速率是0.02 mol·l-1·s-1求:
CO2+H2,在最初5秒钟内,一氧化碳的平均反应速率是0.02 mol·l-1·s-1求:
(1) 5秒钟末,容器内CO2和H2O蒸汽浓度分别为________,__________。
(2) 若设计此反应为一个原电池,则负极发生________反应(填“氧化”,“还原”),负极消耗的物质化学式为____________。
有两种气体单质Am和Bn,已知2.4克Am和2.1克Bn所含有的原子个数相同,分子个数比为2:3;又知A和B的原子核内质子数都等于中子数,且A原子中的L层电子数是其K层电子数的3倍,则A元素的元素符号为________,B元素的元素符号为_________,m=_________;A和B形成红棕色化合物化学式为_________。