乙醛(CH3CHO)在催化剂存在的条件下,可以被空气氧化成乙酸。依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体)。已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次,反应基本完全。有关物质的沸点见下:
| 物质 |
乙醛 |
乙酸 |
甘油 |
乙醇 |
水 |
| 沸点/℃ |
20.8 |
117.9 |
290 |
78.2 |
100 |
请回答下列问题:
(1)试管A内在60℃~80℃时发生的主要反应的化学方程式为(注明反应条件)
_________________________________________。
(2)如图所示,在实验的不同阶段,需要调整温度计在试管A内的位置,在实验开始时温
度计水银球的位置应在________;当试管A内的主要反应完成后温度计水银球的位置应在_______。
(3)烧杯B内盛装的液体可以是_______。
(4)试管C中收集到的是粗产品,若想进一步提纯,可采用的方法是_____;
提纯后的产品若在质谱仪中进行测定,其质荷比最大是____(填数值);
若在核磁共振仪中进行测定,其核磁共振氢谱共有__种峰,峰面积之比为__。
下图所示装置可用来制取Fe(OH)2和观察Fe(OH)2在空气中被氧化时的颜色变化。实验时必须使用铁屑、6 mol/L H2SO4溶液和NaOH溶液。填写下列空白: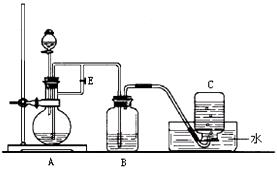
(1)B中盛有一定量的,A中应预先加入的试剂是,
A中反应的化学方程式为。
(2)实验开始时应先将活 塞E(填“打开”或“关闭”),目的是
塞E(填“打开”或“关闭”),目的是
。
(3)A反应一段时间后将活塞E(填“打开”或“关闭”),目的是 。
。
(4)实验结束,拔去装置B中的橡皮塞,使空气进入,Fe(OH)2被氧化。若反应过程中转移了0.04mol电子,则参加反应的氧气的体积为L(标准状况)。
用18mol/L 浓硫酸配制100ml 3.0mol/L 稀硫酸的实验步骤如下:①计算所用浓硫酸的体积,②量取一定体积的浓硫酸,③溶解,④转移、洗涤,⑤定容、摇匀。回答下列问题:
(1)所需浓硫酸的体积是(保留到小数点后一位),量取浓硫酸所用的量筒的规格是(从下列中选:A. 10ml B. 25ml C. 50ml D. 100ml)
(2)在上述实验步骤中,需要用到玻璃棒的有(填序号)。
(3)第⑤步实验的操作是:继续向容量瓶注入蒸馏水至离刻度线1-2cm处,改用胶头滴管向容量瓶滴加至为止。塞紧瓶塞,倒转摇匀。
(4)下列情况对所配制的稀硫酸浓度有何影响?(填“偏大”、“偏小”或“无影响”)
A. 容量瓶用蒸馏水洗涤后残留有少量的水
B. 所用过的烧杯、玻璃棒未洗涤
(10分)1,2 — 二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度2.18 g·cm-3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂.在实验室中可以用下图所示装置制备1,2- 二溴乙烷.其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水).
填写下列空白:
(1)写出本题中制备1,2-二溴乙烷的两个化学反应方程式.
___________________________________________________________
___________________________________________________________
(2)安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞.请
写出发生堵塞时 瓶b中的现象._________________________________.
瓶b中的现象._________________________________.
(3)容器c中NaOH溶液的作用是:__________________________________.
(4)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超过许多.如果装置的气密性没有问题,试分析其可能的原因:_______________________________________________________
________________________________________________________
(10分)某校化学兴趣小组采用酸碱中和滴定法测定学校新购入的烧碱的纯度(烧碱中含有不与酸反应的杂质),试根据实验回答。
(1)实验步骤为:①用托盘天平准确称量4.1g烧碱样品。
②将样品配 成250ml待测液,需要的仪器除玻璃棒、量筒、烧杯外还需要的玻璃仪器有______________________。
成250ml待测液,需要的仪器除玻璃棒、量筒、烧杯外还需要的玻璃仪器有______________________。
③用________、量取10.00ml待测 液,注入锥形瓶中。
液,注入锥形瓶中。
④在锥形瓶中滴入2~3滴________(填指示剂),用0.2010 mol/L的标准盐酸滴定待测烧碱溶液,滴定时左手旋转____式滴定管的玻璃活塞,右手不停地摇动锥形瓶,两眼注视___________,直到滴定终点。
(2)实验过程中,下列操作将造成待测烧碱溶液浓度偏高的是_______________。
①量取待测液的滴定管没有用待测液润洗②锥形瓶水洗后又用待测液润洗
③未用标准盐酸溶液润洗滴定管④滴定过程中振荡时有液滴溅出
⑤滴定前盛装标准盐酸溶液的滴定管尖嘴部分无气泡,滴定后有气泡
⑥滴定前仰视读数,滴定后俯视读数
(3)该小组测得下列数据
| 滴定次数 |
待测液体积/ml |
标准盐酸体积/ml |
|
| 滴定前读数/ml |
滴定后读数/ml |
||
| 第一次 |
10.00 |
0.20 |
22.90 |
| 第二次 |
10.00 |
0.50 |
20.40 |
| 第三次 |
10.00 |
4.00 |
24.10 |
| 第四次 |
10.00 |
0.00 |
20.00 |
根据上述数据,计算烧碱的纯度______________。
某兴趣小组设计出下图所示装置来改进教材中“铜与硝酸反应”实验,以探究化学实验的绿色化。
(1)实验前,关闭活塞b,试管d中加水至浸没长导管口,塞紧试管c和d的胶塞,加热c。其目的是。
(2)在d中加适量NaOH溶液,c中放一小块铜片,由分液漏斗a向c中加入2 mL浓硝酸。c中反应的化学方程式是。再由a向c中加2 mL蒸馏水,c中的实验现象是。
(3)下表是制取硝酸铜的三种方案,能体现绿色化学理念的最佳方案是。理由是_____________。
方案 |
反应物 |
| 甲 |
Cu、浓HNO3 |
| 乙 |
Cu、稀HNO3 |
| 丙 |
Cu、O2、稀HNO3 |
(4)该小组还用上述装置进行实验证明氧化性KMnO4>Cl2>Br2。操作步骤为,实验现象;但此实验的不足之处是。